Descifrando los latidos del corazón para el diagnóstico de enfermedades cardiovasculares
El corazón humano es una maravilla de la ingeniería biológica. Bombea sangre a través del cuerpo día tras día, año tras año. Pero ¿qué ocurre cuando este órgano vital muestra signos de problemas? Aquí es donde entran en juego las señales mecánicas que el corazón emite y que pueden ser fundamentales en el diagnóstico de enfermedades cardiovasculares.
Durante varios años las enfermedades del corazón han sido la principal causa de muerte en México y son un grave problema de salud pública con un alto costo económico asociado. En 2022 y de acuerdo con el Instituto Nacional de Estadística y Geografía (INEGI), del total de muertes registradas (847 mil 716), el 23.6% se atribuyeron a enfermedades del corazón. Dentro de esta categoría, las enfermedades isquémicas, caracterizadas por la reducción del flujo sanguíneo al corazón por bloqueo parcial o total de las arterias, representaron la mayoría, con un 76.5% (152 mil 960 casos). Los trastornos hipertensivos ocuparon el segundo lugar con 14.2% (28 mil 494 casos) seguidas de las relacionadas con la circulación pulmonar y otras enfermedades del corazón, con 9.0% (17 mil 960 casos). Por ello, es importante el uso y desarrollo de técnicas no invasivas para el diagnóstico y tratamiento en estos pacientes, como la electrocardiografía que registra la actividad eléctrica del corazón mediante el electrocardiograma (ECG).
El corazón es un órgano vital del sistema cardiovascular que se encarga de bombear la sangre oxigenada e impulsar su circulación a todo el cuerpo. Para realizar estas funciones, el corazón genera continuamente impulsos eléctricos que son transmitidos por su sistema de conducción eléctrica haciendo que sus cuatro cámaras (dos aurículas y dos ventrículos) se contraigan en sucesión ordenada de tal forma que la contracción auricular (sístole auricular) va seguida de la contracción de los ventrículos (sístole ventricular) y durante la diástole todas las cámaras están relajadas. Para la conexión entre las diferentes cámaras, el corazón tiene cuatro válvulas que se abren y cierran en los instantes adecuados para asegurar que la sangre fluya solo en una dirección y evitar que retroceda (Rodrigo López, 2009). Estas válvulas se clasifican en dos grupos: auriculoventriculares (AV): válvula mitral y válvula tricúspide; y semilunares: válvula sigmoidea aórtica y válvula sigmoidea pulmonar.
Como el latido del corazón y el bombeo de la sangre generan vibraciones en el cuerpo, éstas pueden ser detectadas por transductores ubicados en su superficie, conocidos como wearables, o elementos en contacto directo con el cuerpo, como sillas, camas o básculas. Estas vibraciones han sido investigadas por más de cien años y las señales resultantes han sido denominadas de diversas maneras según el método de registro y la posición del sensor. Actualmente, el balistocardiograma (BCG), además del sismocardiograma (SCG) y el fonocardiograma (FCG) que se describirán a continuación, son las señales más consideradas en este ámbito, ya que proporcionan información de la actividad mecánica del corazón y son utilizadas en combinación con el ECG.
Sismocardiograma (SCG): vibraciones mecánicas que cuentan una historia
El SCG mide las vibraciones cardiacas de baja frecuencia (menores de 25 Hz) que son transmitidas a la pared del tórax, y se compone de varios puntos característicos (Figura 1): cierre de la válvula mitral (MC), apertura de la válvula aórtica (AO), inicio de la inyección rápida (RE), cierre de la válvula aórtica (AC), apertura de la válvula mitral (MO), pico del llenado rápido (RF) y sístole auricular (AS). Estos marcadores son cruciales para analizar la actividad cardíaca y evaluar su salud.
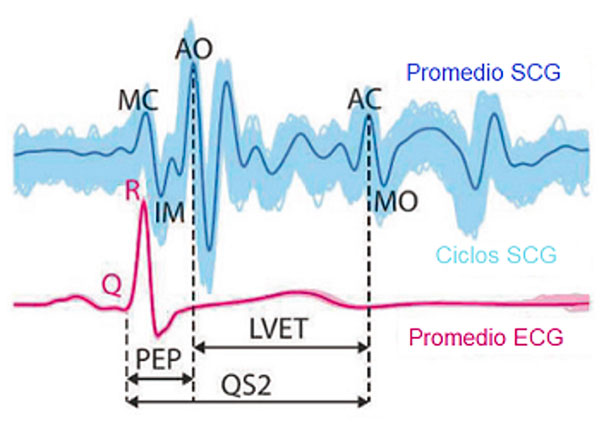
Se ha demostrado la utilidad del SCG en la estimación de intervalos cardíacos como el periodo de pre-eyección (PEP) y el tiempo de eyección del ventrículo izquierdo (LVET). Tanto el PEP como el LVET, son índices significativos que se utilizan ampliamente para evaluar el rendimiento del corazón (Sieciński & Kostka, 2017). El PEP representa el tiempo entre el inicio de la despolarización ventricular y el comienzo de la eyección ventricular, mientras que el LVET es un indicador de la contractilidad cardíaca y está influenciado por el sistema nervioso autónomo. Para calcular el PEP se mide desde el inicio de la onda Q del ECG hasta el pico AO del SCG (primer componente de alta velocidad). El LVET es determinado midiendo el tiempo entre los momentos de apertura y cierre de la válvula aórtica en el ciclo cardíaco.
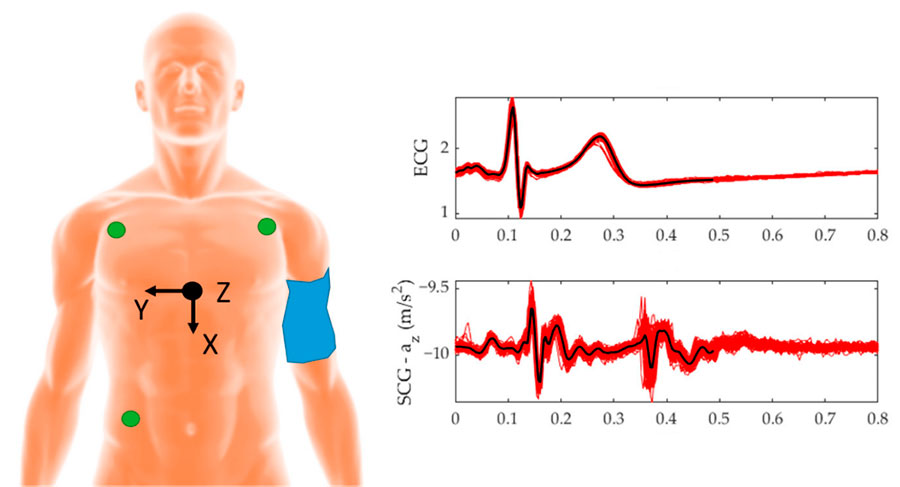
Algunos sistemas que se han desarrollado están compuestos de sensores comerciales mediante una unidad de medición inercial (IMU) colocada en la región de la apófisis xifoides del esternón (Figura 2). Esta disposición permite detectar las vibraciones y movimientos asociados con la actividad cardíaca de manera precisa. Estudios recientes demuestran que se puede detectar el SCG utilizando el acelerómetro de un teléfono móvil, un avance conocido como “m-SCG” (Landreani et al., 2018). Esto abre nuevas posibilidades para el monitoreo y diagnóstico de problemas cardiovasculares de manera más accesible y útil.
El SCG posee la capacidad de detectar algunas de las enfermedades cardiovasculares más comunes a nivel general, como la fibrilación auricular, isquemia del miocardio y hemorragia cardiaca. Esta capacidad sugiere su uso potencial como dispositivo de detección en pacientes cardiacos de alto riesgo. Un amplio estudio multicéntrico demostró que cuando se utilizaban los resultados combinados del ECG y el SCG, la precisión en la predicción de la enfermedad coronaria aumentaba de manera significativa en comparación con los resultados obtenidos solamente a partir del ECG (Wilson et al., 1993). En algunas aplicaciones, como pacientes con quemaduras, con infecciones contagiosas e incluso bebés prematuros, no resultaría factible colocar electrodos para ECG adhesivos o sensores de SCG debido a su complejidad. Por ello, se están investigando técnicas de detección del SCG sin contacto, lo que sería una mejora con respecto al SCG adquirido por sensores de contacto.
Fonocardiograma (FCG): escuchando la música del corazón
Una de las técnicas más antiguas, utilizada por el médico para el diagnóstico cardiovascular, es la auscultación, que consiste en escuchar los sonidos producidos por los órganos y vasos del cuerpo por medio del estetoscopio. El estetoscopio permite establecer un compartimiento de aire cerrado entre una región del tórax de la persona y el oído del médico. Sin embargo, este método es subjetivo, ya que depende totalmente de la capacidad de audición del médico. Aunque la auscultación todavía es el principal método para la detección y análisis de los sonidos cardíacos, existe otra técnica conocida como la fonocardiografía que utiliza un micrófono como transductor de estos sonidos integrado en un estetoscopio que elimina la interpretación subjetiva del médico.
Esta técnica registra en forma gráfica los sonidos cardíacos producidos por vibraciones de alta frecuencia (mayores de 25 Hz) generados por el corazón y por los grandes vasos sanguíneos, debido a la apertura y cierre de las válvulas cardiacas, así como del flujo de la sangre; por ello es utilizada en el diagnóstico de enfermedades valvulares. Estos sonidos se clasifican en dos categorías: ruidos y soplos cardiacos (Vermarien, 2006). Como una evolución de la tecnología de la auscultación cardiaca, estos registros se adquieren en sincronía con el ECG para comparar las relaciones temporales entre estos sonidos y los eventos mecánicos y eléctricos del ciclo cardíaco (Wen et al. 2014).
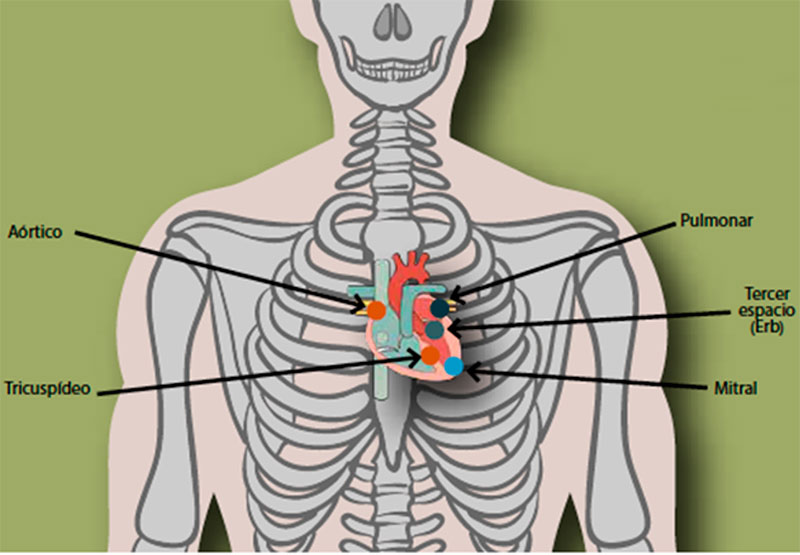
Para detectar el epicentro de los principales ruidos cardiacos existen cinco focos principales de auscultación del tórax: aórtico, pulmonar, aórtico accesorio o de Erb, tricúspideo y mitral (Figura 3).
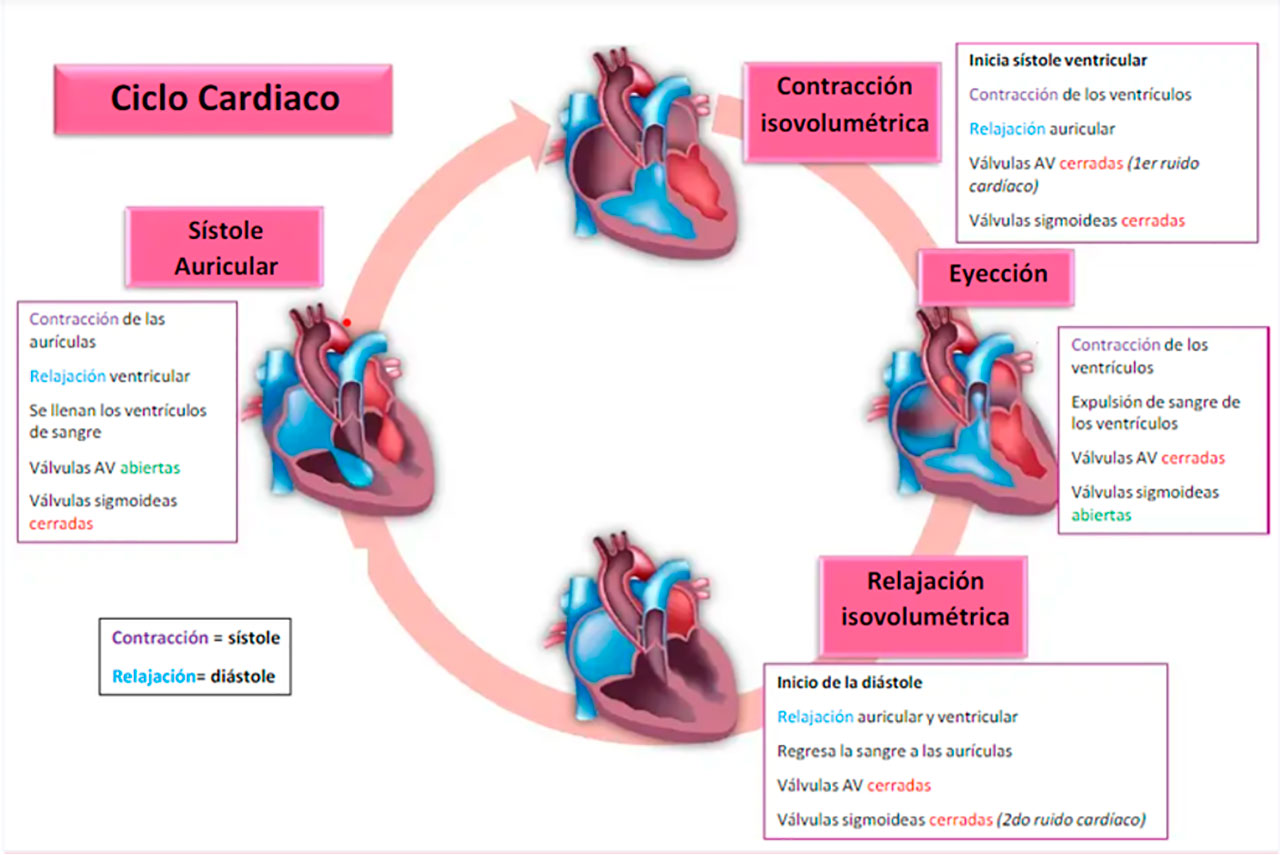
La Figura 4 muestra cómo se producen los ruidos S1 y S2 durante el ciclo cardíaco debido a la coordinación de la contracción y relajación de las aurículas y ventrículos, la apertura y cierre de las 4 válvulas cardíacas y el flujo de sangre. Estos ruidos se escuchan en situaciones normales durante la auscultación con el estetoscopio.
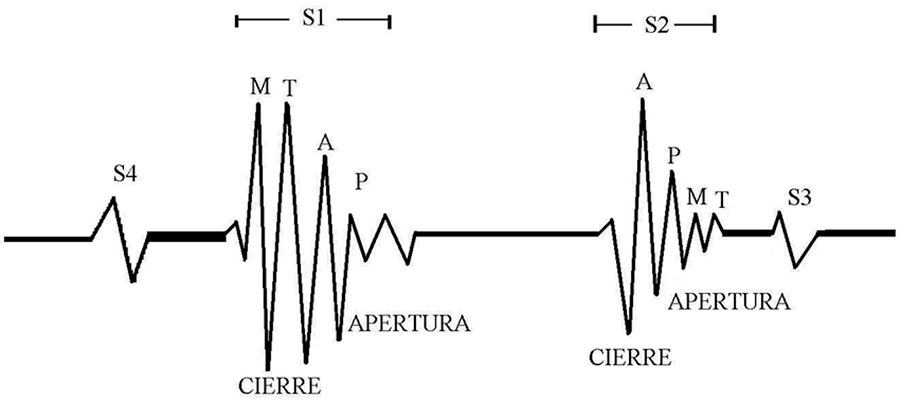
La figura 5 muestra los tipos de ruidos cardiacos y su origen. S1 y S2 marcan el inicio y el final, respectivamente de las fases del ciclo cardíaco, sístole y diástole son sonidos de alta frecuencia, mientras que S3 y S4 son de baja frecuencia que pueden escucharse en diversas afecciones. S3 indica el llenado rápido de ventrículos (diástole temprana), y está asociado a una dilatación ventricular (insuficiencia cardíaca congestiva). S4 representa el llenado tardío de los ventrículos por contracción auricular (diástole tardía) y está asociado a ventrículos no distensibles o rígidos. Las letras M (mitral), T (tricúspide), A (aortica) y P (pulmonar) señalan el cierre y la apertura de las válvulas. Estos ruidos son vibraciones o sonidos causados por la aceleración y desaceleración del flujo sanguíneo.
En este examen clínico no solo se escuchan los ruidos cardiacos, también pueden oírse los pulmones e incluso el sonido que produce el flujo sanguíneo de los vasos. La distinción entre el FCG y los sonidos pulmonares se basa en la ubicación de la auscultación, los tipos de sonidos, la relación con el ciclo cardíaco o respiratorio, la instrumentación utilizada y las fuentes de sonido. La auscultación cuidadosa y la comprensión de las características específicas de cada uno ayudarán en la diferenciación efectiva.
Con respecto a los soplos cardiacos, se trata de vibraciones o sonidos debido a la turbulencia del flujo sanguíneo, el cual se produce por el cambio de un flujo laminar a un flujo turbulento. Esto indica una disminución del área valvular (estenosis) o que la válvula no cierra correctamente y ocasiona reflujo (regurgitación o insuficiencia valvular). Los soplos son más prolongados que los ruidos cardíacos; son agudos y ásperos, a menudo contienen 2 o 3 componentes separados y pueden variar su posición corporal; pueden ser sistólicos, diastólicos o continuos. Pueden clasificarse en función de su intensidad, localización y ubicación respecto al momento del ciclo cardíaco. En un paciente con taquicardia pueden ser casi continuos. Los soplos se clasifican en intensidad en una escala de 1 al 6 (Tabla 1).

En conclusión, el SCG y el FCG se han revelado como herramientas poderosas en la detección temprana y el monitoreo de enfermedades cardiovasculares en combinación con el ECG. La capacidad de detectar sutiles alteraciones en la mecánica cardíaca, incluso antes de que se manifiesten los síntomas clínicos, brinda una oportunidad sin precedentes para una intervención temprana y un tratamiento más efectivo. Si bien aún existen desafíos en términos de estandarización y disponibilidad generalizada, el SCG y el FCG prometen una perspectiva útil en el diagnóstico y el tratamiento de enfermedades cardiovasculares, mejorando así la calidad de vida y la salud de la población.
Referencias
Rodrigo López, J. L. (2009). Válvulas cardíacas: funcionamiento y enfermedades. En A. López Farré, & C. Macaya Miguel, Libro de la salud cardiovascular del Hospital Clínico San Carlos y de la Fundación BBVA (págs. 457-462). Bilbao: Fundación BBVA.
Sieciński, S., & Kostka, P. (2017). Determining Heart Rate Beat-to-Beat from Smartphone Seismocardiograms: Preliminary Studies. Advances in Intelligent Systems and Computing, 133–140. doi:10.1007/978-3-319-70063-2_15
Landreani, F., Caiani, E. G., Golier, D., Hossein, A., Rabineau, J., Migeotte, P., & Van de Borne, P. (2018). Heartbeat Detection Using Three-Axial Seismocardiogram Acquired by Mobile Phone. Computing In Cardiology. https://doi.org/10.22489/cinc.2018.215
D’Mello, Y., Skoric, J., Xu, S., Roche, P. J. R., Lortie, M., Gagnon, S., & Plant, D. V. (2019). Real-Time Cardiac Beat Detection and Heart Rate Monitoring from Combined Seismocardiography and Gyrocardiography. Sensors (Basel, Switzerland), 19(16), 3472. https://doi.org/10.3390/s19163472
Wilson, R. A., Bamrah, V. S., Lindsay, J., Jr, Schwaiger, M., & Morganroth, J. (1993). Diagnostic accuracy of seismocardiography compared with electrocardiography for the anatomic and physiologic diagnosis of coronary artery disease during exercise testing. The American journal of cardiology, 71(7), 536–545. https://doi.org/10.1016/0002-9149(93)90508-a
Vermarien, H. (2006). Phonocardiography. En J. G. Webster, Encyclopedia of Medical Devices and Instrumentation (págs. 278-290). Hoboken, New Jersey: John Wiley & Sons.
Wen, Y.-N., Pui-Wai Lee, A., Fang, F., Jin, C.-N., & Yu, C.-M. (2014). Beyond auscultation: Acoustic cardiography in clinical practice. International Journal of Cardiology, 172(3), 548-560. doi:10.1016/j.ijcard.2013.12.298
Cruz Ortega, H. A., & Calderón Monter, F. J. (2016). El corazón y sus ruidos cardíacos. Revista de la Facultad de Medicina (México), 59(2), 49-55. Recuperado el 16 de abril de 2024, de http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S0026-17422016000200049&lng=es&tlng=es
Tamborini, V. (8 de Septiembre de 2021). Scribd. Recuperado el 16 de Abril de 2024, de https://es.scribd.com/document/523793588/Ciclo-cardiaco
Cerquera Soacha, E. (2005). Caracterización de estados funcionales en fonocardiografía empleando análisis acústico y técnicas de dinámica no lineal. Tesis de Maestría, Universidad Nacional de Colombia Facultad de Ingeniería y Arquitectura, Departamento de Ingeniería Eléctrica, Electrónica y Computación, Manizales. Recuperado el 16 de Abril de 2024, de https://repositorio.unal.edu.co/handle/unal/3482
Fonseca-Sánchez, L. A., Bobadilla-Aguirre, A., & Espino-Vela, J. (2015). Soplo normal, inocente o inorgánico. Acta pediátrica de México, 36(1), 50-54. Recuperado el 16 de Abril de 2024, de http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S0186-23912015000100009&lng=es&tlng=es