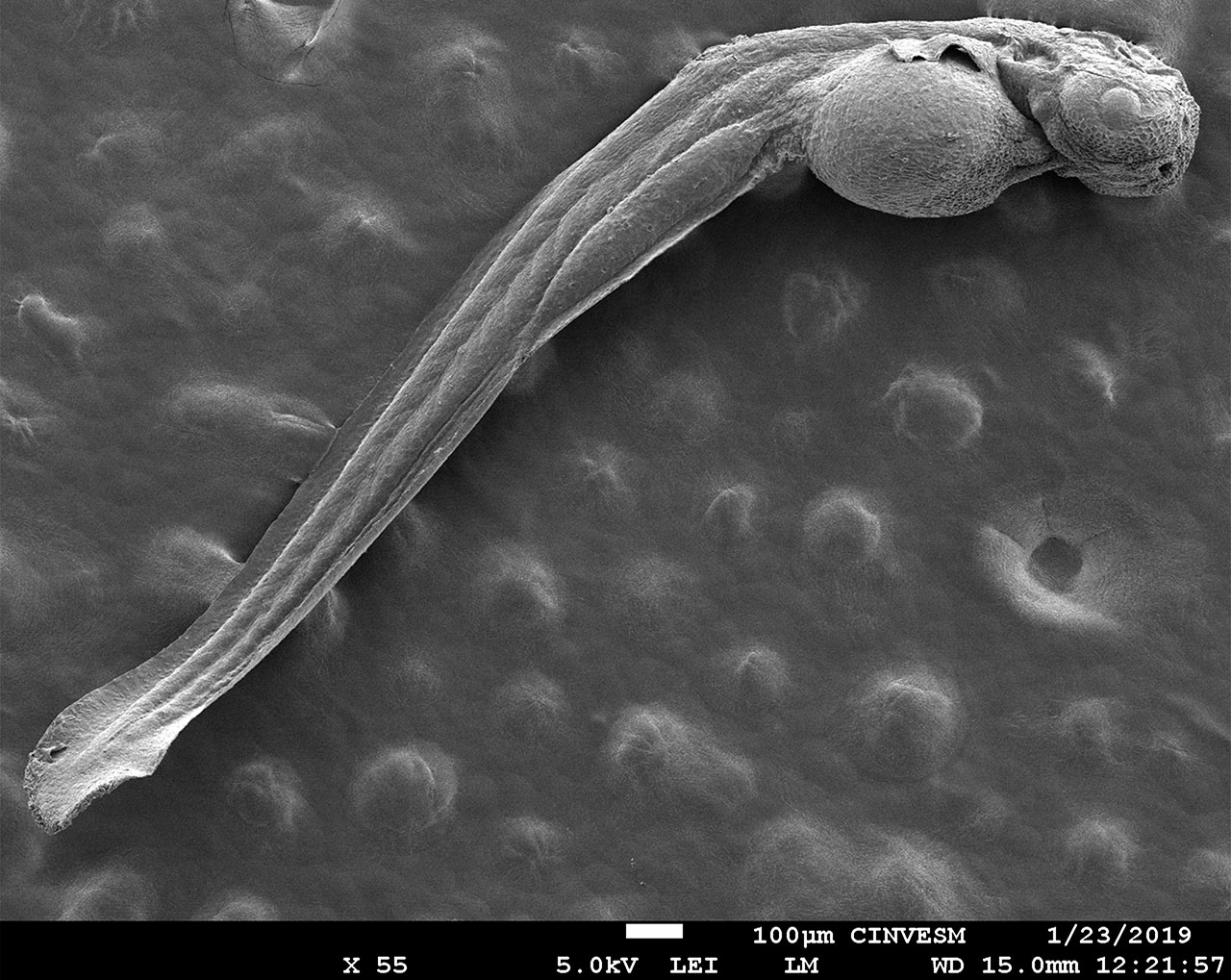
Crecimos con el mito de Prometeo robando el fuego de los dioses para obsequiarlo a los humanos, un acto que lo condenó a un terrible castigo. Imaginamos al héroe encadenado observando cómo un ave rapaz devoraba su hígado, el cual se regeneraba diariamente. Hoy sabemos que la regeneración hepática podría no ser necesariamente un castigo.
Re-descubriendo al hígado
El hígado, tanto humano como el de otros animales, realiza funciones como la síntesis de proteínas y lípidos, regula el metabolismo de la glucosa, almacena energía y favorece la desintoxicación del organismo; por ello las enfermedades que afectan a este órgano, tales como hepatitis, cirrosis, cánceres, y daños por trastornos metabólicos, son de gran relevancia clínica.
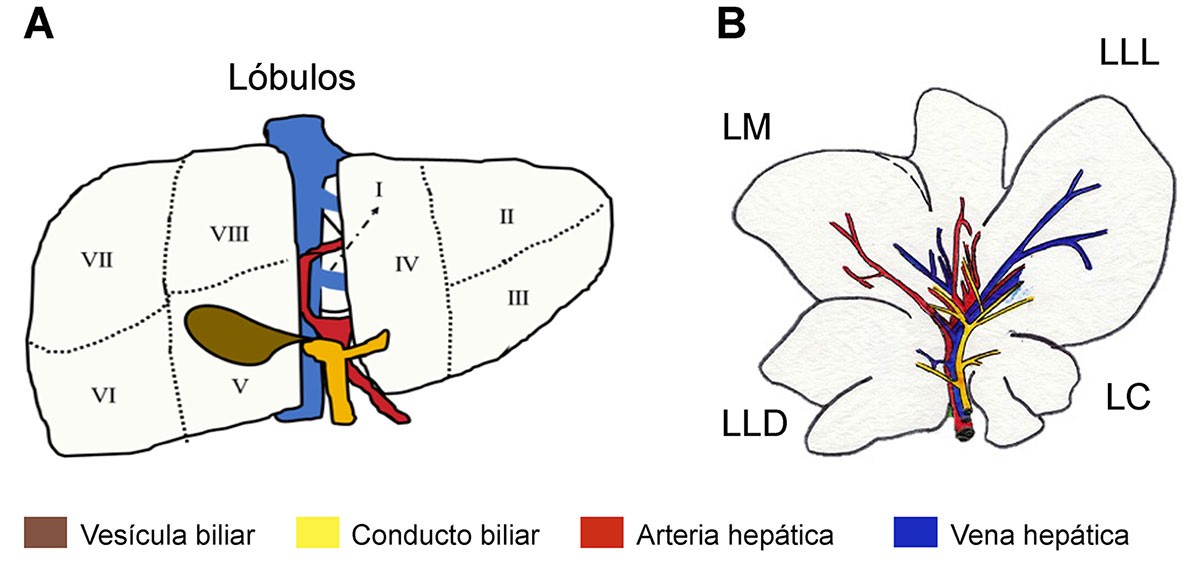
En el ser humano, este órgano tiene un peso aproximado de 1.5 Kg; se encuentra en la parte superior derecha del abdomen, debajo del diafragma y posee un característico color marrón rojizo debido a la abundante irrigación sanguínea que recibe. 1.5 litros de sangre pasan por el hígado cada minuto, de la cual el 75% proviene de la vena porta, que traslada sangre poco oxigenada que recoge nutrientes y toxinas absorbidas por el sistema gastrointestinal, mientras que el 25% procede de la arteria hepática con sangre oxigenada. Anatómicamente el hígado está integrado por 2 lóbulos organizados en 8 segmentos según Claude Couinaud (Figura 1) y se encuentra recubierto de una capa de tejido conjuntivo fibroso denominada Cápsula de Glisson.
El hígado de la rata es similar al del humano, por ello se ha establecido como modelo para la experimentación pre-clínica; está integrado por 4 lóbulos denominados lóbulo caudado (LC), lóbulo lateral derecho (LLD), lóbulo medio (LM) y el lóbulo lateral izquierdo (LLI), que en conjunto poseen una forma similar a la de una flor y representa el 4.15% del peso total del animal, es decir el hígado de una rata de 250 g de masa corporal pesa alrededor de 10 g. A diferencia del ser humano, la rata no posee una vesícula biliar; no obstante, su hígado cuenta con conductos biliares, rodeados de extensa irrigación sanguínea y nerviosa (Figura 1).
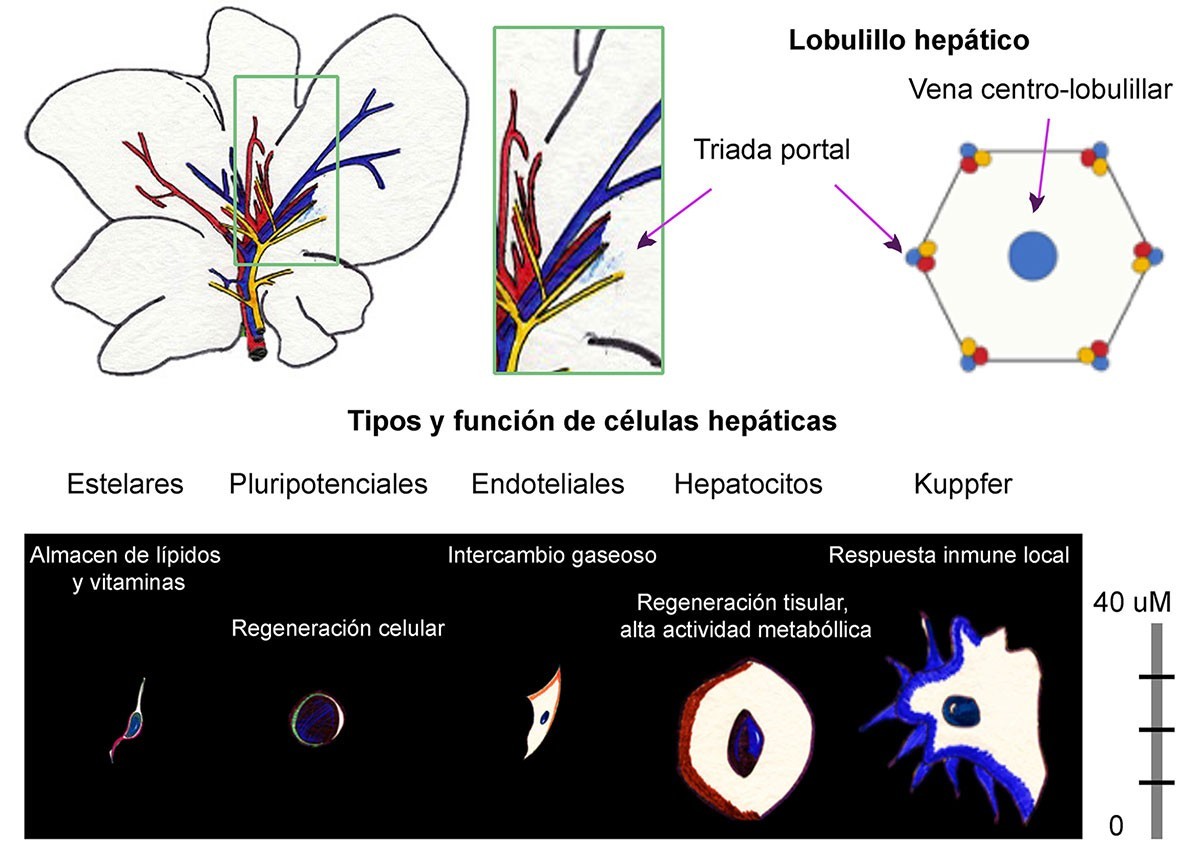
Cada lóbulo hepático se divide en cientos de miles de lobulillos, los cuales albergan diferentes tipos de células. Estos lobulillos poseen en cada una de sus esquinas una rama de la triada portal, la cual es un sistema de flujo sanguíneo constituido por el conducto biliar, una rama de la arteria hepática y ramas de la vena hepática (Figura 2). Esta irrigación facilita el flujo de sangre, nutrientes y productos de desecho, los cuales viajan por medio de los sinusoides hepáticos, que son una especie de capilares que van desde la periferia del lobulillo hepático hasta su centro, en donde desembocan en una vena centro-lobulillar que es donde se recogen los productos secretados por los hepatocitos. A su vez, la comunicación de los hepatocitos que se encuentran dispuestos en forma radial a la vena centro-lobulillar con los sinusoides, se produce por medio del espacio perisinusoidal (o espacio de Disse) donde se lleva a cabo el intercambio de nutrientes.
Las células de hígado y su función
El parénquima hepático, es un tejido con gran riqueza celular; está constituido por hepatocitos, células de Kupffer, células ovales, células endoteliales fenestradas y las células de Ito, así como tejido graso y conjuntivo y pequeños capilares. Todos estos elementos se ordenan dentro de los lobulillos hepáticos (Figura 2).
Cada una de las células que integran al hígado posee características morfológicas y funciones especiales, por ejemplo, los hepatocitos, células que miden entre 20 y 30 micrómetros, que pueden tener uno o más núcleos esféricos de gran tamaño y conforman el 80% del volumen del hígado. Estas células representan la unidad funcional del órgano, debido a que facilitan la síntesis de proteínas, procesos de desintoxicación, metabolismo de fármacos, almacenamiento de moléculas energéticas, por lo que poseen alta capacidad de proliferación como estrategia para revertir el estrés celular. Por otra parte, se han descubierto algunas células que pueden tener la función de células madre; son las células ovales, las cuales tienen un núcleo y citoplasma ovoide (> 8 µm), provienen de los canales de Hering que invaden el parénquima y son estructuras que enlazan a los sinusoides con el conducto biliar actuando como medio para drenar la bilis, por lo que la alteración de la dinámica de células ovales y de los hepatocitos pudieran potenciar el cáncer, aunque esto depende de múltiples factores, como el estado metabólico, la nutrición, la predisposición genética y el entorno ambiental.
Otros grupos de células que habitan el hígado son las células endoteliales fenestradas, las células de Kupffer y las células de Ito. Las endoteliales revisten los sinusoides y permiten el intercambio directo de substancias entre la sangre y los hepatocitos. Las células de Kupffer son macrófagos, es decir son un tipo de células de defensa; su función radica en eliminar partículas tóxicas producidas por las demás células o las bacterias; además tienen la función de “presentar” dichas partículas a otras células del sistema inmunológico. Por su parte, las células de Ito o estrelladas, tienen un tamaño aproximado de 1 a 2 µm y su función principal es el almacenamiento de lípidos y vitamina A. En años recientes, estas células han sido de mucho interés para los científicos, pues se ha sugerido que participan en la remodelación de la matriz extracelular durante la regeneración hepática.
Regeneración hepática y salud
El fenómeno de la regeneración hepática es conocido desde finales del siglo XIX, y gracias a los científicos Higgins y Anderson que crearon un protocolo experimental en animales de laboratorio en 1931 llamado hepatectomía parcial (HP), se ha podido estudiar con mayor detalle la dinámica celular y molecular de la recuperación anatómica y funcional del hígado. Hasta mediados de 2021, alrededor de 2 millones de publicaciones han reportado el uso de este modelo, y tan solo en el último año se han aceptado más de 300 publicaciones de este tópico. La HP consiste en una cirugía bajo anestesia y condiciones apropiadas de asepsia, en la que se corta cierto porcentaje del hígado (del 5 al 95%); es una herramienta útil para el tratamiento de diversas patologías como la cirrosis, y recientemente se ha empleado como estrategia para la modalidad de donantes de órganos vivos, pues el tiempo de espera para un trasplante de hígado puede demorar meses y hasta años, mientras que un trasplante de donante vivo de hígado puede disminuir estos tiempos.
Cuando la HP se utiliza como estrategia en los trasplantes de donantes vivos, sus porcentajes pueden variar, pero siempre se debe asegurar que el volumen hepático residual del donador sea al menos el 30% del volumen hepático nativo. Además, los lóbulos removidos por la cirugía varían en función de si es un niño o un adulto quien recibe el trasplante. Países de Europa y Asia utilizan esta nueva modalidad de donación en la mayoría de los trasplantes de hígado, y México ha ido incursionando en este ámbito, siendo los estados de Jalisco, CDMX y Chihuahua donde se han realizado más cirugías en instituciones públicas y privadas.
Cabe destacar que el protocolo diseñado por Higgins y Anderson ha sufrido modificaciones en los porcentajes de hígado removido y se ha utilizado en diversos modelos animales, destacando estudios en conejos, perros, monos, ratones, cerdos y ratas, siendo estas últimas las más empleadas porque su costo de mantenimiento es bajo y generan camadas grandes (10-20 crías por parto) y por su utilidad en abordajes farmacológicos, toxicológicos, etológicos, metabólicos, y quirúrgicos, sobresaliendo su importancia en estudios de investigación básica y traslacional.
Se ha descubierto que las HP menores a 90% permiten la supervivencia de los animales sin afectación en la capacidad motriz, de gestación, metabólicas ni fisiológicas; esto es posible porque después de la HP existe recuperación anatomofuncional del hígado, y se ha descrito que a mayor porcentaje de remoción del lóbulo hepático, se incrementa la velocidad de regeneración. El uso de HP ha permitido profundizar en los fenómenos que ocurren dentro de la regeneración hepática, donde se destacan procesos de estrés celular, proliferación, muerte por apoptosis, adaptación celular y remodelación tisular. Sin embargo, la HP al ser una cirugía conlleva riesgos; en el marco clínico se ha reportado que los pacientes sometidos a este procedimiento desarrollan complicaciones menores como la formación de queloides (cicatrices resaltadas en la zona de la cirugía), pérdida de peso, o de mayor gravedad como infecciones, hernias, complicaciones biliares y hemorragias.
Los científicos que estudian los mecanismos de daño hepático en modelos animales han encontrado que la regeneración del hígado se debe a su extraordinaria capacidad de proliferación celular, la cual es favorecida por la producción y liberación de sustancias denominadas factores de crecimiento, además de la bilis, y hormonas como la insulina. Los factores de crecimiento son sustancias producidas naturalmente por nuestro cuerpo y se encuentran reguladas en función del estímulo. En el caso de la regeneración hepática, se ha identificado que los factores de crecimiento de hepatocitos, epidérmico, transformante, necrosis tumoral alfa y fibroblastos, estimulan la proliferación de hepatocitos, células endoteliales y promueven la diferenciación celular. Otras sustancias implicadas son las citosinas, como la interleucina 6 y el neurotransmisor noradrenalina, estimulando la respuesta inmunológica y la síntesis de factores de crecimiento.
El fenómeno de la regeneración hepática es muy complejo e incluso involucra la activación de circuitos neuronales. El hígado está inervado, lo cual permite el intercambio de información de la cavidad abdominal con el encéfalo. La comunicación hígado-encéfalo se lleva a cabo a través de una red nerviosa llamada plexo hepático, que a su vez es una parte de otra red más grande denominada plexo solar que conecta al cerebro con el hígado por medio del nervio vago (Figura 3).
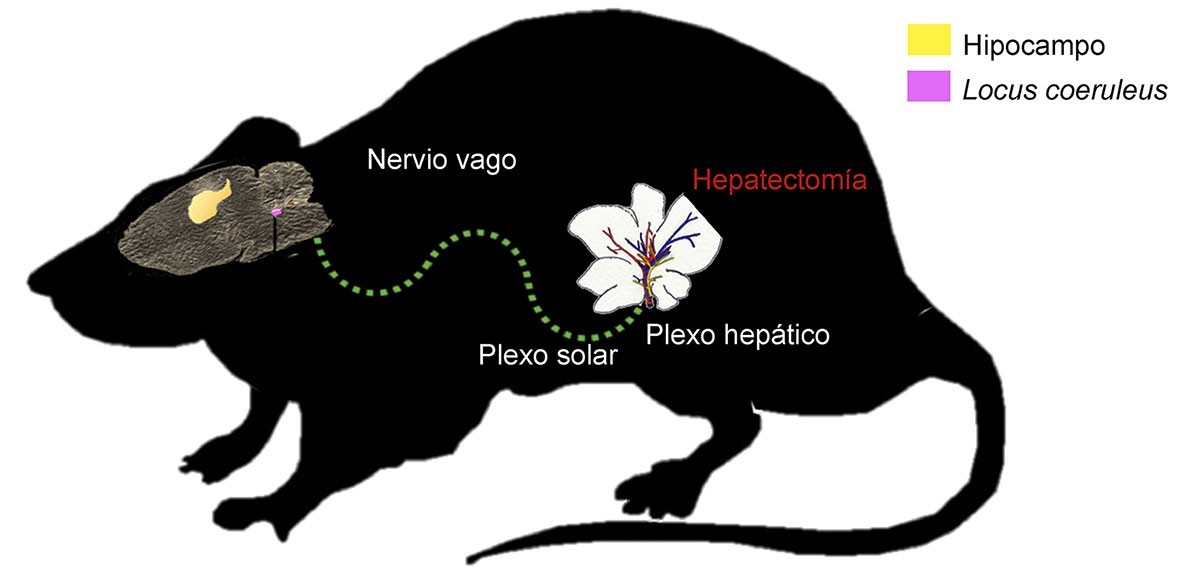
En ratas, dentro de los hallazgos más notables relacionados con la HP y el cerebro, se ha observado que la HP disminuye la expresión génica de receptores GABA y serotoninérgicos, implicados en diversos mecanismos en el cuerpo; además favorece la pérdida de espinas dendríticas, lo que implica alteraciones de la memoria; se ha descubierto que también promueve el aumento de activación microglial en el hipocampo, desencadenando el proceso neuroinflamatorio. También estudios recientes indican que áreas cerebrales como el locus coeruleus, principal productor del neurotransmisor noradrenalina, está relacionado con el proceso de regeneración al estimular la producción de factores de crecimiento hepático. Sin duda, la interacción bidireccional entre el cerebro con órganos como el hígado, y el conocimiento de los mecanismos celulares específicos que explican su capacidad de regeneración, da pauta al ingenio de los científicos para explorar novedosas estrategias terapéuticas, y nos deja la certeza de que el mito de Prometeo es un recordatorio de que hay castigos que pueden salvar vidas.
Referencias
- Aller, M. A., Arias, N., Prieto, I., Agudo, S., Gilsanz, C., Lorente, L., & Arias, J. (2012). A half century (1961-2011) of applying microsurgery to experimental liver research. World journal of hepatology, 4(7), 199-208.
- Cienfuegos, J. A., Rotellar, F., Baixauli, J., Martínez-Regueira, F., Pardo, F., & Hernández-Lizoáin, J. L. (2014). Liver regeneration–the best kept secret. A model of tissue injury response. Revista española de enfermedades digestivas: organo oficial de la Sociedad Española de Patologia Digestiva, 106(3), 171-194.
- González, E. J. D., González, K. S. D., Cisneros, C. M., & Prieto, L. R. P. (2019). Consideraciones prácticas y fisiológicas de la regeneración hepática en el trasplante. Revista Repertorio de Medicina y Cirugía, 28(3), 152-156.
- Jensen, K. J., Alpini, G., & Glaser, S. (2013). Hepatic nervous system and neurobiology of the liver. Comprehensive Physiology, 3(2), 655-665.