Inmunoterapia de células CAR T: una nueva alternativa para el cáncer
Introducción
Los seres humanos estamos compuestos de billones de células que a través del transcurso de nuestras vidas crecen y se reproducen de acuerdo con las necesidades que el cuerpo requiera para realizar un sinfín de procesos metabólicos, bioquímicos y celulares. En condiciones normales, una célula controla su crecimiento por división celular (proliferación y ciclo celular), homeostasis en los tejidos (diferenciación y metabolismo), alteraciones en su material genético (mutaciones) y cuando debe morir (apoptosis). Cuando una célula presenta alguna anomalía en uno o varios de estos procesos, surge el cáncer, ocasionando que las células anormales (células tumorales) se reproduzcan descontroladamente, modificando la función de los tejidos donde se originan o en otras partes del cuerpo. El sistema inmunológico tiene la capacidad de combatir estas células tumorales para evitar su proliferación y migración hacia otros órganos, evitando la formación de metástasis. Sin embargo, el sistema inmunológico puede tener fallas en el reconocimiento, control y/o eliminación de las células cancerosas, ocasionando afectaciones a los diferentes órganos del cuerpo.
El sistema inmunitario de una persona es muy complejo e implica diferentes tipos de células y sistemas en todo el cuerpo. En las células del sistema inmunitario se encuentran los glóbulos blancos, que son los encargados de defender al organismo de patógenos y/o células tumorales, una subpoblación de glóbulos blancos se denomina linfocitos. Existen dos principales tipos de linfocitos, los linfocitos B (encargados de producir anticuerpos contra los patógenos) y los linfocitos T, que representan el mayor porcentaje del total de linfocitos. A su vez, los linfocitos T se pueden dividir en linfocitos T CD4+, orquestadores de la respuesta de las células inmunes, y linfocitos T CD8+ que normalmente son responsables de destruir células infectadas por virus o células cancerosas.
En México durante 2020, el cáncer provocó más de 90 mil muertes y más de 195 mil nuevos casos; la Agencia Internacional para la Investigación sobre el Cáncer, perteneciente a la Organización Mundial de la Salud (OMS), estima que para 2040 el número de nuevos casos registrados en nuestro país se incrementará en un 65%, alcanzando a más de 323 mil personas. De acuerdo con el Instituto Nacional de Estadística y Geografía (INEGI), el cáncer se coloca como la cuarta causa de muerte en México, con el 8.3% del total de las defunciones, en donde la anemia, neutropenia y eventos óseos, son los principales padecimientos relacionados o derivados del tratamiento contra el cáncer (INEGI, 2020). Como indican estos datos, el cáncer es un grave problema de salud, por lo que se ha buscado la manera de combatirlo mediante el uso de nuevos tratamientos, como las inmunoterapias de células CAR T.
¿Qué es una inmunoterapia de células CART y cómo funciona?
La inmunoterapia es un tipo de tratamiento biológico en el que se estimulan las defensas naturales del sistema inmunitario para combatir de mejor manera el cáncer; ya que refuerza o cambia el funcionamiento del sistema inmunitario para que elimine las células cancerosas. Para el tratamiento contra el cáncer se emplean diferentes tipos de inmunoterapias como: fármacos inhibidores de puntos de control inmune, anticuerpos monoclonales dirigidos contra blancos específicos de células cancerosas, sustancias inmunomoduladoras de la respuesta inmune, vacunas que fortalecen la respuesta contra células cancerosas y transferencia de células T (más activas o modificadas “células CART T”) del propio paciente.
La inmunoterapia de células CART surge como una alternativa prometedora mediante el uso de linfocitos T con el receptor de antígeno quimérico, CAR por sus siglas en inglés. Los CAR son receptores artificiales de linfocitos T creados mediante ingeniería genética. Se llaman quiméricos porque están elaborados con partes de diferentes anticuerpos. Por lo tanto, esta terapia se basa en ayudar al sistema inmunitario de una persona con cáncer, modificando de forma genética a sus linfocitos T para que expresen el receptor CAR; los cuales son dirigidos a un antígeno específico de las células cancerosas, haciendo que los linfocitos T estén mejor equipados para encontrar y acabar con las células cancerosas.
Producción de células CAR T
El sistema inmunitario puede reconocer células cancerosas en el cuerpo mediante la búsqueda de proteínas llamadas “antígenos” en la superficie de estas células. Los linfocitos T poseen sus propias proteínas que actúan como “receptores”. La relación entre antígenos y receptores inmunes es como una cerradura y una llave. Al igual que una cerradura solo se puede abrir con la llave correcta, cada antígeno extraño tiene un receptor inmune único que puede unirse a él. Por lo tanto, los receptores que se unen a los antígenos de superficie ayudan a provocar que otros componentes del sistema inmunitario destruyan las células con tales antígenos. Sin embargo, si las células inmunitarias no tienen los receptores adecuados, no pueden adherirse a los antígenos y ayudar a destruirlas. Por lo que la producción de células CAR T es una forma de mejorar al sistema inmunológico, añadiendo los receptores necesarios y específicos a los linfocitos T para atacar esas células.
La manera de generar células CAR T usadas en las inmunoterapias para mejorar la respuesta inmune del paciente, es mediante una extracción de sangre, separación de sus células sanguíneas y posterior aislamiento de únicamente linfocitos T. Estos últimos se modifican genéticamente en el laboratorio agregándoles un gen específico encargado de expresar el receptor quimérico de antígenos (CAR), el cual ayuda a las células T a adherirse a un antígeno en específico de las células cancerosas. Éstas se cultivan en equipos especiales para multiplicarlas y generar una cantidad óptima para las condiciones de la persona enferma. Finalmente, las células CAR T generadas son introducidas en el paciente.
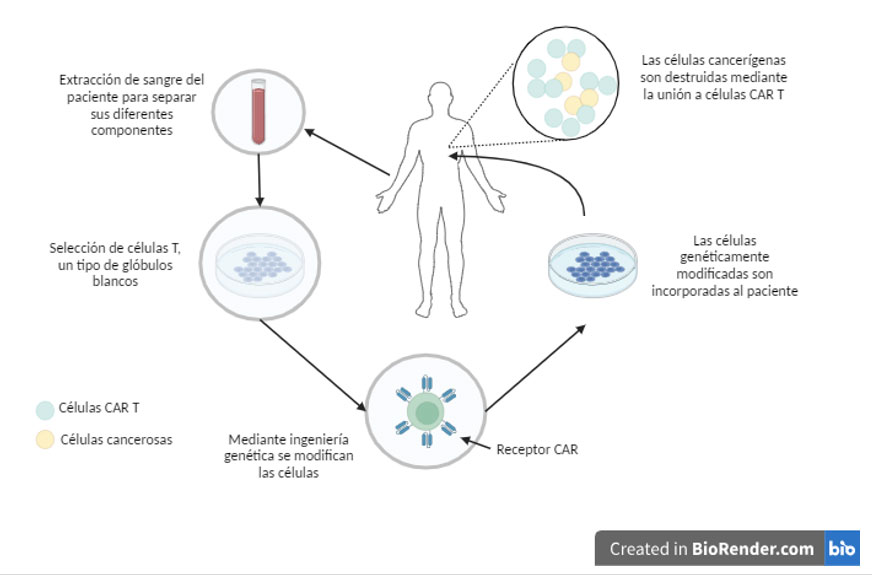
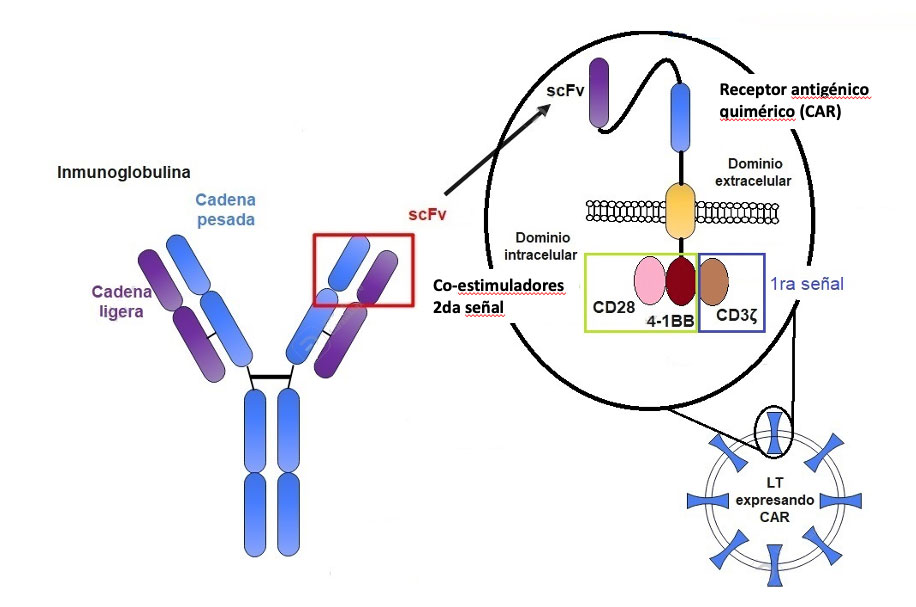
Células CAR T y su mecanismo de acción
En el ejemplo que usamos, “la cerradura” es el receptor quimérico, formado por tres dominios: extracelular, transmembranal, e intracelular. El dominio extracelular está constituido por el receptor con la capacidad de unirse a “la llave”, que en este caso es el antígeno de la superficie de las células tumorales. Esta cerradura contiene regiones de reconocimiento antigénico (denominadas scFv). Cuando se genera un primer contacto entre el antígeno cancerígeno (la llave) y el dominio extracelular (la cerradura), el dominio intracelular envía dos señales de activación. Por un lado, los dominios coestimuladores (CD28, 4-1BB, etcétera) proporcionan una importante señal para la activación, proliferación y producción de los linfocitos T; mientras que CD3ζ interviene en la transducción de señales y la expresión de los receptores de células T (TCR) en la superficie de la célula. Los linfocitos CAR T activados se multiplican y envían otras señales a diferentes partes del sistema inmunitario para que lleguen al lugar de la célula cancerosa. Estas proteínas de señalización se llaman citocinas. Todas las citocinas y linfocitos T activados provocan entonces una inflamación significativa centrada en la célula cancerosa, lo que causa la muerte de la célula. Si todas las células cancerosas mueren, el cáncer puede entrar en remisión, lo que significa que ha desaparecido temporal o de forma permanente.
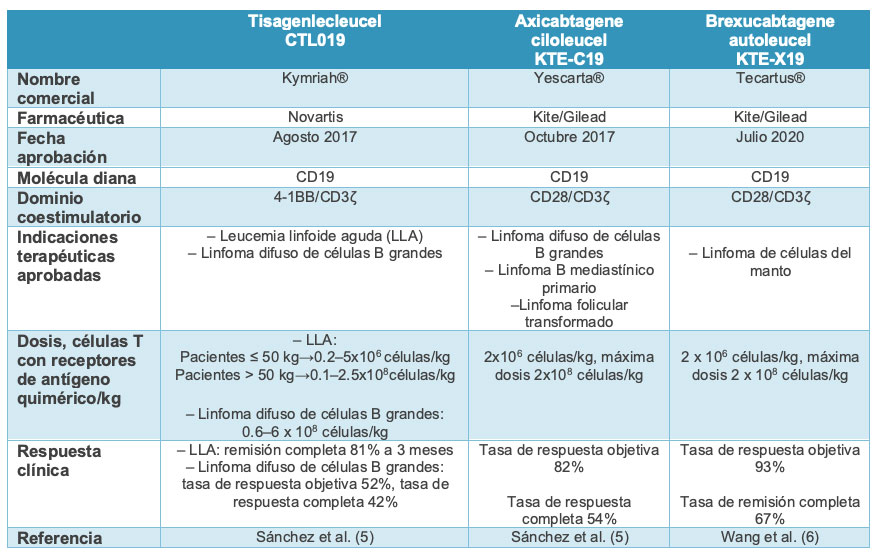
Terapias CAR-T aprobadas por la FDA
Actualmente se encuentran aprobados tres diseños de terapias CAR-T por parte de la Food and Drug Administration (FDA) de Estados Unidos:
– Tisagenlecleucel (nombre comercial Kymriah®). Es un agente CAR-T contra CD19 que usa 4-1BB/CD3ζ como dominio coestimulatorio. Desarrollado por el laboratorio Novartis y la Universidad de Pensilvania. Se emplea para el tratamiento de pacientes jóvenes con Leucemia linfoblástica aguda de precursores B refractarias y en adultos con linfoma no Hodgkin B difuso de células grandes (LBDCG) refractarios a dos o más líneas de tratamientos.
– Axicabtagene ciloleucel (nombre comercial Yescarta®). Es un agente CAR-T contra CD19 de segunda generación que utiliza CD28 como dominio coestimulatorio. Desarrollado por la farmacéutica Kite/Gilead. Ha sido evaluado en pacientes adultos con LBDCG refractarios, con linfoma B mediastínico primario o linfoma folicular transformado.
– Brexucabtagene autoleucel (nombre comercial Tecartus®). Es una terapia celular dirigida contra CD19. Al igual que el axicabtagene ciloleucel, Tecartus® fue desarrollado por Kite/Gilead. Recientemente fue aprobado por la FDA para el tratamiento del linfoma de células del manto refractario.
 El 30 de agosto de 2017, la FDA aprobó la terapia de células CAR-T para el tratamiento en niños con Leucemia linfoide aguda (LLA) y en adultos con ciertos tipos de leucemia no Hodking (LNH), específicamente linfoma difuso de células B grandes, linfoma folicular, linfoma folicular transformado, linfoma primario de mediastino y linfoma del manto. A pesar de los grandes avances, existen todavía retos a los que se enfrenta esta terapia como, por ejemplo, encontrar la molécula adecuada para dirigir la fracción de reconocimiento del receptor quimérico, ya que son antígenos que también suelen expresarse en los tejidos normales. Se ha experimentado con varias moléculas, pero la que mayor efectividad ha tenido es la terapia CAR-T contra CD19 para tratar los tumores de células B.
El 30 de agosto de 2017, la FDA aprobó la terapia de células CAR-T para el tratamiento en niños con Leucemia linfoide aguda (LLA) y en adultos con ciertos tipos de leucemia no Hodking (LNH), específicamente linfoma difuso de células B grandes, linfoma folicular, linfoma folicular transformado, linfoma primario de mediastino y linfoma del manto. A pesar de los grandes avances, existen todavía retos a los que se enfrenta esta terapia como, por ejemplo, encontrar la molécula adecuada para dirigir la fracción de reconocimiento del receptor quimérico, ya que son antígenos que también suelen expresarse en los tejidos normales. Se ha experimentado con varias moléculas, pero la que mayor efectividad ha tenido es la terapia CAR-T contra CD19 para tratar los tumores de células B.
El futuro de las células CAR T
Este nuevo tipo de terapia, basada en transferencia de linfocitos T modificados con receptores CAR, ha instaurado un amplio potencial para el futuro de la medicina moderna. Actualmente, la aplicación del principio de CAR-T en diferentes campos se encuentra en fase de investigación. Dentro de las posibles aplicaciones resaltan enfermedades infecciosas como la adquirida por virus de inmunodeficiencia humana (VIH), en donde se han encontrado resultados prometedores en estudios de laboratorio, requiriendo que sean reproducidos en modelos vivos de latencia de VIH inducido por terapia antirretroviral; procesos fibróticos por medio de la ablación de fibroblastos al dirigir las células CAR-T contra la proteína de activación de fibroblastos, en casos como fibrosis cardiaca; trasplantes de órganos y autoinmunidad, en donde se ha demostrado que podrían ser usadas como células T regulatorias específicas de antígeno para ayudar a establecer tolerancia al trasplante y reestablecerla en enfermedades autoinmunes.
Comentarios finales
La terapia de linfocitos T con receptores quiméricos (CAR T) constituye un gran avance en el área de la oncohematología. Es la primera forma de terapia de transferencia génica diseñada para obtener aprobación comercial por la FDA. Esta inmunoterapia se ha desarrollado rápidamente en los últimos años. En la actualidad está prescrita para el tratamiento de procesos linfoproliferativos y representa una esperanza para pacientes que sufren de tumores sólidos. Las limitaciones de la selección de pacientes, el síndrome de liberación de citocinas, el síndrome de neurotoxicidad y mejora de la respuesta, son objetivos por resolver en los que se trabaja actualmente.
Bibliografía
Cuenca, J. A., Schettino, M. G., Ver, K. E., & Tamariz, L. E. (2022). Terapia de células T con receptores de antígenos quiméricos: revisión de la literatura. Gaceta mexicana de oncología, 21(1), 17-25.
De Ozalla, C. B. A. (2022). Visión actual de la terapia con células CAR-T. Revista de Investigación y Educación en Ciencias de la Salud (RIECS), 7(1), 83-90.
Gamberale, R. (2014). CAR T cells: Fundamentos de esta prometedora terapia inmunológica. Hematología, 18, 28-31.
Instituto Nacional de Estadística y Geografía. (2021). Estadísticas a propósito del día mundial contra el cáncer. INEGI. 105(21), 2-3.
Sánchez-Escamilla M, Yáñez San Segundo L, Urbano-Ispizua A, Perales M-A. Células CAR T: el futuro ya es presente. Med Clin (Barc). 2019; 152:281-6.
Wang M, Munoz J, Goy A, Locke FL, Jacobson CA, Hill BT, et al. KTE-X19 CAR T-Cell therapy in relapsed or refractory mantle-cell lymphoma. N Engl J Med. 2020; 382:1331-42.