La lucha continúa: el desafío para el desarrollo de un tratamiento para el dengue
El 28 de marzo de 2024, la Organización Panamericana de la Salud (OPS) mediante un comunicado de prensa, señaló su preocupación por el grave aumento de casos de dengue en las Américas. Las cifras no mienten; en marzo de este año se reportaron más de 3 millones de personas afectadas en la región, es decir, 3 veces mayor al número de pacientes notificados en marzo de 2023, por lo que se prevé un récord en el número de casos totales de dengue al final del año.
En México, el pronóstico se está cumpliendo ya que hasta la semana epidemiológica 34 (18-24 de agosto) del 2024 se reportaron 41,923 casos de dengue. Es razonable suponer que el principal responsable de este número es la temporada cálida y lluviosa que se presenta en los meses de junio, julio, agosto y septiembre que favorece la propagación del mosquito Aedes (vector responsable de la transmisión del virus dengue (DENV) y causante de la enfermedad). Sin embargo, al comparar con la misma semana del año 2023 (13,025 casos) se observa que el número de casos en 2024 incrementó más del doble respecto al año anterior.
Es un hecho que las personas enfermas de dengue aumentan cada año, y por increíble que parezca, a pesar de los avances tecnológicos, no ha sido posible la creación de un antiviral seguro y eficaz para combatir esta enfermedad que afecta al mundo desde hace más de 40 años. En algunos pacientes la enfermedad puede ser asintomática, en otros se limita a signos y síntomas leves y un cierto número de personas (alrededor del 5%) puede presentar un cuadro clínico caracterizado por fuga de plasma, shock hipovolémico, trombocitopenia y hemorragia, que ponen en grave peligro su vida hasta ocasionar la muerte (Lim, 2019). Debido al poco éxito en el desarrollo de un antiviral contra el dengue, el manejo y tratamiento a los pacientes se limita a reposo en cama, reposición de líquidos corporales mediante fluidoterapia por vía oral o intravenosa (según lo requiera), y analgésicos y antipiréticos que únicamente tienen como objetivo aliviar los síntomas y hacer sentir mejor al paciente.
¿Qué hace la comunidad científica para combatir esta enfermedad? ¿qué tan cerca estamos de desarrollar un tratamiento para el dengue?
Para contestar estas preguntas debemos saber que la comunidad científica ha convertido el desarrollo de fármacos antivirales contra dengue en una prioridad en la investigación, ya que es una de las principales herramientas para luchar contra este problema de salud pública. El desarrollo de fármacos antivirales es un problema complejo, especialmente porque tienen que considerarse diversos aspectos de índole económica, social y cultural, y otros factores relacionados con la biología del virus y del humano, que desafían directamente el desarrollo de una terapia.
En el dengue, la investigación farmacológica se vuelve una tarea más difícil, ya que enfrentamos a cuatro diferentes serotipos del virus (DENV-1, DENV-2, DENV-3 y DENV-4) que, aunque son virus similares a nivel genético, la infección con uno de los serotipos no solo no protege contra los otros tres, sino que puede favorecer las formas graves de la enfermedad. Por lo tanto, un fármaco ideal para el tratamiento del dengue debería tener actividad antiviral contra los cuatro serotipos, capacidad de resolver rápidamente los síntomas, evitar las formas graves de la enfermedad, causar toxicidad nula o mínima en el ser humano, no interaccionar con otros compuestos, producción a gran escala, bajos costos, y tolerabilidad en un amplio rango de la población como en mujeres embarazadas y pacientes con comorbilidades como diabetes e hipertensión (Lim, 2019; Palanichamy Kala et al., 2023).
Aun cuando los desafíos parecen muchos, el desarrollo farmacéutico en el dengue no es imposible y se ha centrado principalmente en dos estrategias generales. La primera consiste en diseñar y descubrir fármacos dirigidos hacia los componentes del virus y sus funciones. Las proteínas blanco pueden formar parte de la partícula viral (proteínas estructurales) o ser producidas durante la infección (proteínas no estructurales), para generar nuevos virus, es decir, los tratamientos deben de ser capaces de inhibir o bloquear las funciones de las principales proteínas virales necesarias para producir la infección.
Dado que estos fármacos se dirigen al virus específicamente, suelen ser muy poco tóxicos, y los efectos secundarios que pueden producir son mínimos para el humano. Sin embargo, su desventaja es que van perdiendo efectividad a lo largo del tiempo por las rápidas mutaciones del virus, por lo que poco a poco se seleccionan los virus más resistentes. Así, las proteínas virales blanco a las que se han dirigido la mayoría de los fármacos contra dengue son: las proteínas estructurales C y E que juegan un papel importante en la unión, entrada, ensamblaje y formación de las nuevas partículas virales; la proteína NS3 (no estructural) que es la proteasa encargada de generar a las proteínas virales maduras; NS5 que tiene actividad principalmente de polimerasa y se ocupa de replicar el genoma viral y NS4B, que funciona como un factor clave en la inhibición de la respuesta inmune contra el DENV (García et al., 2017; Lee et al., 2023; Lim et al., 2013; Palanichamy Kala et al., 2023; Sundar et al., 2022). En la siguiente tabla se muestran algunos compuestos o fármacos que han demostrado potencial antiviral mediante el bloqueo de las funciones de las proteínas virales del DENV (Figura 1).
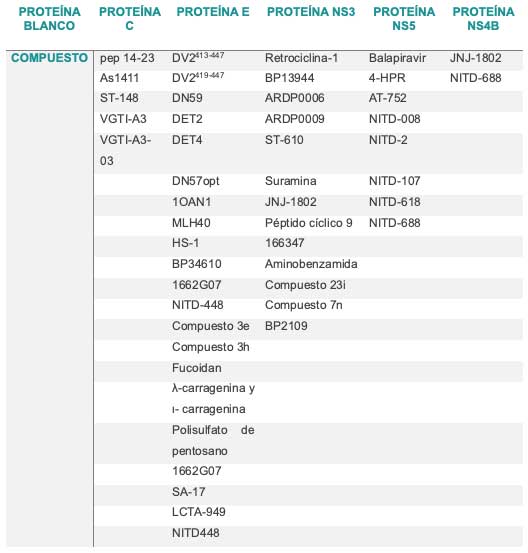
A pesar de que hasta ahora se han evaluado muchos compuestos dirigidos contra los componentes virales, ninguno de ellos ha llegado a ser administrado en pacientes con éxito.
La segunda estrategia para desarrollar un antiviral requiere conocer los mecanismos y factores que el DENV utiliza de la célula humana para poder replicarse. En otras palabras, esta estrategia pretende limitar la disponibilidad de los componentes celulares que usa el virus para así impedir el desarrollo de la infección. Debido a su naturaleza, estos tratamientos evitan la resistencia a los fármacos y, puesto que diversos virus pueden usar estos componentes celulares en su beneficio, esta estrategia funciona para el diseño de antivirales de amplio espectro, aunque pueden tener mayor probabilidad de causar toxicidad y efectos adversos en los pacientes. No obstante, al tratarse de una enfermedad aguda, la presencia de reacciones perjudiciales por el uso continuo del fármaco sería escasa. Dentro de esta estrategia se ha llegado a evaluar algunos compuestos o fármacos con potencial antiviral como los que se muestran en la tabla 2 (Lee et al., 2023; Lim, 2019; Lim et al., 2013; Palanichamy Kala et al., 2023).
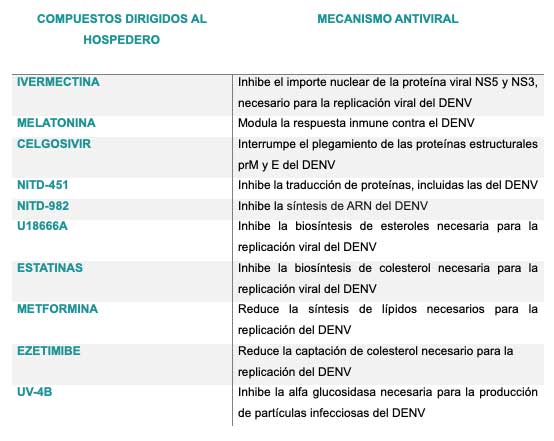
Es importante mencionar que aunque los compuestos enlistados anteriormente no demostraron ser totalmente seguros o efectivos para combatir el dengue, se ha identificado que los principales problemas que han limitado su uso son: toxicidad alta, falta de eficacia o potencia, escasa selectividad, propiedades farmacocinéticas limitadas, ausencia en la mejora de los síntomas y que algunos tienen efecto antiviral in vitro, pero no en pruebas in vivo, o tienen efecto terapéutico in vivo en animales de laboratorio, pero lamentablemente no en humanos (Palanichamy Kala et al., 2023).
Aunque todo luce como un escenario gris ante la búsqueda del tan anhelado antiviral, los grandes esfuerzos hechos hasta hoy han servido para entender, analizar e intentar solucionar el problema, mejorando y optimizando nuevos fármacos que siguen estas estrategias, y no solo eso, sino que ha permitido encontrar nuevas plataformas para el desarrollo de antivirales, tales como el reposicionamiento de fármacos (Figura 2). Esta estrategia sirve para aprovechar los conocimientos previos sobre la seguridad de los fármacos ya aprobados por las diferentes entidades regulatorias, que son comercializados para otras enfermedades y donde se evalúan cuáles de ellos son capaces de inhibir la infección por dengue.
Esta clase de estrategia permite reducir el gasto económico y el tiempo para cumplir con todas las fases necesarias para la aprobación de un fármaco. Por otro lado, la combinación de varios fármacos dirigidos a diferentes blancos es una estrategia novedosa con buenos resultados que puede mejorar la eficacia de los tratamientos contra el dengue. Adicionalmente, el uso de tecnologías de alto rendimiento como el virtual screening y el uso de la inteligencia artificial sirven como herramientas capaces de acelerar la identificación de compuestos con actividad antiviral, es decir, con la implementación correcta de diversas estrategias y tecnologías estamos más cerca de encontrar este antiviral.

No debe olvidarse que el control de una enfermedad como el dengue requiere de actuar en diversos frentes y no solo con el desarrollo de un antiviral. La prevención de la población en riesgo de infectarse mediante el monitoreo correcto de los mosquitos con insecticidas, con el uso de mosquitos modificados genéticamente y mosquitos infectados con el género de bacterias Wolbachia que reducen su capacidad para propagar el virus, así como la descacharrización (eliminación de los criaderos de los mosquitos transmisores de dengue), el diagnóstico clínico adecuado y la vigilancia de los pacientes, son estrategias que tenemos a la mano que son igual de importantes para enfrentar este problema.
En resumen, el panorama es alentador y la expectativa por un tratamiento farmacológico seguro y eficaz se vuelve cada vez más prometedora debido a los importantes avances en la comprensión de la enfermedad, la identificación de nuevas dianas terapéuticas, el surgimiento y uso de nuevas tecnologías y estrategias, y a la colaboración de la comunidad científica con el sector privado, por lo que seguramente un tratamiento antiviral para el dengue podrá estar disponible pronto.
Bibliografía
- García, L. L., Padilla, L., & Castaño, J. C. (2017). Inhibitors compounds of the flavivirus replication process. Virology Journal, 14, 95. https://doi.org/10.1186/s12985-017-0761-1
- Lee, M. F., Wu, Y. S., & Poh, C. L. (2023). Molecular Mechanisms of Antiviral Agents against DengueVirus. Viruses, 15(3), 705. https://doi.org/10.3390/v15030705
- Lim, S. P. (2019). Dengue drug discovery: Progress, challenges and outlook. Antiviral Research, 163, 156-178. https://doi.org/10.1016/j.antiviral.2018.12.016
- Lim, S. P., Wang, Q.-Y., Noble, C. G., Chen, Y.-L., Dong, H., Zou, B., Yokokawa, F., Nilar, S., Smith, P., Beer, D., Lescar, J., & Shi, P.-Y. (2013). Ten years of dengue drug discovery: Progress and prospects. Antiviral Research, 100(2), 500-519. https://doi.org/10.1016/j.antiviral.2013.09.013
- Palanichamy Kala, M., St. John, A. L., & Rathore, A. P. S. (2023). Dengue: Update on Clinically Relevant Therapeutic Strategies and Vaccines. Current Treatment Options in Infectious Diseases, 15(2), 27-52. https://doi.org/10.1007/s40506-023-00263-w
- Sundar, S., Piramanayagam, S., & Natarajan, J. (2022). A review on structural genomics approach applied for drug discovery against three vector-borne viral diseases: Dengue, Chikungunya and Zika. Virus Genes, 58(3), 151-171. https://doi.org/10.1007/s11262-022-01898-5
Ficha de Autor