Introducción
El sueño y la percepción del dolor son fundamentales para la sobrevivencia y el bienestar de los individuos. Ambos fenómenos tienen una relación recíproca y bidireccional. Adicionalmente, estos fenómenos pueden presentarse de manera diferencial entre sexos. Este artículo explora la relación entre la falta de sueño y la hipersensibilidad al dolor, destacando los mecanismos neurobiológicos involucrados y las diferencias específicas entre los sexos en esta interacción.
El sueño y el dolor: Dos mecanismos clave para sobrevivir
¿Por qué el sueño juega un papel importante en nuestro bienestar?, ¿Por qué la calidad del sueño afecta las funciones del organismo?, ¿Cuál es el impacto del sueño dependiendo del sexo de los individuos? Estas son preguntas que vamos respondiendo conforme tenemos mayor conocimiento.
Dormir es una necesidad básica y esencial para la supervivencia. Cuando no conseguimos dormir lo suficiente, podemos enfrentar problemas en nuestra salud. Hasta el momento se sabe que el sueño, como lo experimentamos los seres humanos, se presenta en todos los mamíferos y en otros grupos de vertebrados, lo que demuestra su importancia en la supervivencia. El sueño es vital debido a que durante este proceso se restablece la energía y la regulación de la temperatura; promueve la depuración de desechos celulares, y contribuye a regular la secreción de algunas hormonas, entre otras funciones. El sueño se define como un estado natural y reversible en el que el cuerpo reduce su percepción del entorno y su capacidad de respuesta, adoptando una postura relajada y disminuyendo la actividad física. El sueño es un proceso complejo con alta actividad cerebral que ayuda a recuperar el equilibrio del organismo tras el desgaste del día.
El dolor se define como una experiencia sensorial y emocional desagradable, generada por un daño o amenaza de daño al organismo. El dolor es resultado de un proceso neurobiológico llamado nocicepción, que es un mecanismo sensorial que detecta y nos hace reaccionar a tiempo ante posibles daños o amenazas en el entorno. La detección de estímulos nocivos se realiza a través de neuronas especializadas denominadas nociceptores. Estas neuronas detectan estímulos dañinos y los traducen en impulsos nerviosos que transmiten a neuronas de segundo orden localizadas en la parte posterior de la médula espinal. Estas neuronas espinales envían la información a varias regiones del sistema nervioso central y es en el cerebro donde se genera la sensación del dolor, se identifican detalles como el origen e intensidad y se añade un componente emocional de aversión, angustia y miedo. Por lo tanto, el dolor es una sensación que cada persona experimenta de una forma única y diferente.
La capacidad de sentir dolor, al igual que el sueño, juega un papel crucial en la protección de nuestro cuerpo y en la promoción de la supervivencia. Cuando el sistema nociceptivo detecta un estímulo dañino, experimentamos un dolor rápido y transitorio conocido como dolor nociceptivo, que va acompañado de respuestas motoras automáticas (reflejos), para evitar o reducir el daño. Si el estímulo causa daño en los tejidos, se desencadena el dolor inflamatorio, en el que las células dañadas y las del sistema inmune, liberan sustancias químicas que ayudan a reparar el daño, y también activan los nociceptores. Este dolor inflamatorio tiene una función protectora que favorece la recuperación del tejido dañado. Existe otra clase de dolor que es en sí mismo una patología, normalmente de tipo crónico. En este caso, con frecuencia se manifiestan dolor espontáneo, hipersensibilidad a estímulos dañinos (hiperalgesia) y también hipersensibilidad a estímulos que normalmente se consideran inofensivos (alodinia). El dolor neuropático, por ejemplo, se presenta tras una lesión traumática o enfermedad que afecta el funcionamiento de las áreas del sistema nervioso, implicadas en el procesamiento del dolor. Se encuentra, además, un conjunto de síndromes dolorosos (fibromialgia, dolor inducido por estrés crónico, dolor inducido por falta de sueño, etcétera) denominados dolor nociplástico; en este caso no hay un daño o proceso inflamatorio evidente, sin embargo, se genera una hipersensibilidad dolorosa que puede ser crónica y que disminuye la calidad de vida de las personas que lo padecen.
La conexión entre sueño y dolor
El sueño y el dolor comparten una relación bidireccional y recíproca, es decir, son fenómenos que se afectan mutuamente. Experimentar dolor crónico suele dificultar la conciliación del sueño, modificar la duración y la alternancia ordenada entre sus fases o interrumpir su continuidad. Por otra parte, las alteraciones del sueño tienen una prevalencia muy alta en pacientes que sufren algún tipo de dolor crónico. En estos casos, la mala calidad del sueño intensifica la percepción del dolor, mientras que el aumento de la severidad del dolor dificulta aún más el sueño, creando un círculo vicioso en el que tanto el dolor como la falta de sueño se perpetúan y se amplifican. Varios estudios de investigación llevados a cabo en humanos sanos muestran que la privación de sueño, incluso durante solo una noche, es suficiente para inducir un estado transitorio de hipersensibilidad ante estímulos mecánicos y térmicos. Así mismo, la privación total o restricción parcial de sueño en modelos animales muestra una reducción en los umbrales al dolor.
La falta de sueño provoca un aumento en la sensibilidad al dolor
Los mecanismos detrás de la hipersensibilidad al dolor causada por la falta de sueño, no se comprenden del todo, aunque investigaciones recientes han dado luz a algunos procesos involucrados. Por ejemplo, la privación de sueño aumenta la activación de células inmunes que liberan sustancias proinflamatorias llamadas citocinas que favorecen la activación de los nociceptores. Un efecto similar se observa en las neuronas de segundo orden localizadas en la médula espinal. En este caso, las células gliales —células no neuronales del sistema nervioso— liberan estas sustancias y aumentan la excitabilidad de las neuronas espinales, enviando al cerebro una mayor estimulación que se traduce en un aumento en la percepción del dolor. También la falta de sueño reduce la eficacia de los sistemas naturales de alivio del dolor, como los opioides endógenos (sustancias para el dolor que produce nuestro propio cuerpo), lo que explica por qué fármacos como la morfina –opioide exógeno– reducen su efecto analgésico –disminución del dolor– tras una noche sin dormir. La región del cerebro relacionada con las emociones y la recompensa también se ve afectada; la falta de sueño aumenta la excitabilidad de estas neuronas, incrementando la aversión al dolor. De manera interesante, la adenosina, un neuromodulador que promueve el sueño, parece estar implicada en la hipersensibilidad al dolor, de hecho, la cafeína, un inhibidor de los receptores a adenosina, reduce la nocicepción en modelos animales. Finalmente, la falta de sueño afecta la barrera hematoencefálica que protege al cerebro, aumentando su permeabilidad y permitiendo que moléculas inflamatorias y tóxicas ingresen al sistema nervioso, lo que podría exacerbar el dolor.
Impacto del sexo en la percepción del dolor y los trastornos de sueño
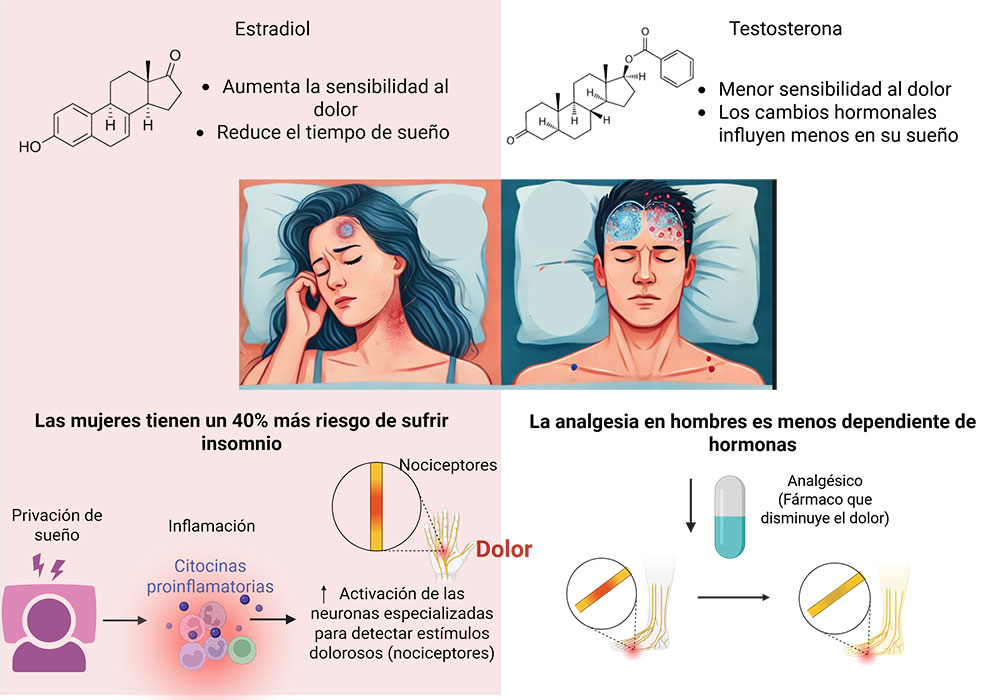
Existe evidencia que indica que la percepción del dolor no es igual entre mujeres y hombres. Por ejemplo, ciertos síndromes de dolor crónico, como la migraña y los trastornos de las articulaciones, tienen una mayor prevalencia en mujeres que en hombres. Uno de los posibles mecanismos involucrados en este fenómeno, lo constituye la presencia de las hormonas sexuales. Respecto al papel de los estrógenos, -hormonas producidas principalmente en los ovarios de las mujeres-, algunos estudios apuntan a que aumentan la sensibilidad al dolor visceral, mientras que otros sugieren que reduce el dolor somático. Estudios en roedores muestran que la ausencia de estrógenos (debido a la extirpación de los ovarios) aumenta la respuesta nociceptiva a estímulos mecánicos y térmicos. En cambio, cuando los niveles de estrógenos se mantienen altos de manera constante, la sensibilidad al dolor disminuye. El papel de los andrógenos, como la testosterona, también se ha puesto de manifiesto en la percepción del dolor. La testosterona reduce el dolor en hombres y mujeres, tanto en estudios humanos como animales, principalmente al modular la inflamación. Sin embargo, la producción secundaria de estrógenos a partir de la testosterona puede complicar la interpretación de los resultados obtenidos con esta hormona.
Los trastornos de sueño no afectan a todos por igual. Las mujeres tienen 40% más de probabilidades de sufrir insomnio a lo largo de su vida, en comparación con los hombres. Durante etapas como la pubertad, el embarazo o la menopausia, los niveles de hormonas como los estrógenos y la progesterona cambian drásticamente en las mujeres y eso tiene efecto en varios procesos fisiológicos. Por ejemplo, durante la menopausia muchas mujeres experimentan insomnio o sueño interrumpido, lo que sugiere que las hormonas sexuales tienen un impacto directo en cómo descansamos. Recientemente se ha demostrado que las mujeres con privación de sueño son más sensibles al dolor térmico y mecánico que los hombres. Esta diferencia podría explicarse por variaciones en los sistemas opioides endógenos —nuestro sistema natural de alivio del dolor— cuyo funcionamiento está modulado por hormonas como el estradiol. Además, la inflamación, otro factor clave en la percepción dolorosa, también se ve afectada por hormonas sexuales. Estos hallazgos subrayan la importancia de considerar las diferencias sexuales tanto en la investigación básica como en el desarrollo de tratamientos analgésicos.
Pero no solo en los humanos se ha observado un efecto diferente entre sexos respecto a la sensibilidad dolorosa inducida por los trastornos de sueño. En estudios con roedores se ha observado que las hembras tienden a dormir menos que los machos, especialmente en la fase de sueño profundo. Sin embargo, cuando se les retiran las hormonas sexuales, estas diferencias desaparecen, lo que confirma su participación. Las hormonas sexuales afectan cuánto y qué tan bien dormimos. En las hembras de roedores, el 17-β-estradiol reduce el tiempo de sueño, especialmente durante la noche. Curiosamente, la testosterona también tiene un efecto similar en las hembras, pero no en los machos. Es posible que parte de esta diferencia se deba a que la testosterona se convierte en estradiol, lo que refuerza la idea de que esta hormona regula el sueño en las mujeres. Aunque los machos también producen estradiol, su sueño parece ser menos sensible a los cambios hormonales. Esto podría explicar por qué, en general, los hombres tienden a dormir mejor que las mujeres.
Implicaciones para la farmacología clínica
Los hallazgos recientes sobre las diferencias sexuales en la percepción del dolor y su relación con el sueño tienen profundas implicaciones para el tratamiento farmacológico. Estudios preclínicos han demostrado que, en modelos de privación de sueño, la activación de los receptores a estrógenos es crucial para que ciertos fármacos ejerzan su efecto analgésico, un hallazgo que explica por qué tratamientos estandarizados pueden fallar en mujeres con desequilibrios hormonales o trastornos del sueño. Estos descubrimientos subrayan la necesidad de adoptar un enfoque personalizado que considere no solo el sexo biológico, sino también el estado hormonal, la calidad del sueño y el contexto psicosocial del paciente. En la práctica clínica, esto se traduciría en ajustar la selección y dosificación de analgésicos, especialmente para mujeres con dolor crónico, donde la interacción entre hormonas, sueño y medicamentos es particularmente relevante para un tratamiento más seguro y eficaz en el manejo del dolor.
Notas finales
Investigar y comprender los mecanismos que subyacen a esta compleja relación entre el sueño y el dolor son la clave para diseñar estrategias de prevención y tratamientos efectivos para el manejo clínico de los pacientes afectados por algún trastorno de sueño, y para evitar en ellos el desarrollo de dolor crónico y viceversa. Asimismo, tener la perspectiva de que la regulación del sueño y la percepción del dolor no son iguales entre sexos y que las hormonas sexuales intervienen en su regulación, es relevante para diseñar tratamientos más eficaces para mujeres y hombres. El conocimiento de este campo de estudio debe difundirse para generar conciencia en la población sobre la importancia de cuidar los hábitos del sueño en el mantenimiento de la salud.
Lecturas recomendadas
Alexandre C, et al. (2017). Decreased alertness due to sleep loss increases pain sensitivity in mice. Nature Medicine 23:768-774.
Haack M, et al. (2019). Sleep deficiency and chronic pain: potential underlying mechanisms and clinical implications. Neuropsychopharmacology 45:205-216.
Hambrecht-Wiedbusch V, et al. (2017). Preemptive caffeine administration blocks the increase in postoperative pain caused by previous sleep loss in the rat: a potential role for preoptic adenosine A(2A) receptors in sleep-pain interactions. Sleep 40: zsx116.
Kourbanova K, Alexandre C, Latremoliere A. (2022). Effect of sleep loss on pain, new conceptual and mechanistic avenues, Frontiers in Neuroscience 16:1009902.
Medina-Flores F, et al. (2020). Sleep loss disrupts pericyte-brain endothelial cell interactions impairing blood-brain barrier function. Brain, Behavior and Immunity 89:118-132.
Sarajari, S., Oblinger, M.M. (2010). Estrogen effects on pain sensitivity and neuropeptide expression in rat sensory neurons. Experimental Neurology, 224(1):163-169.
*Foto de portada creada con Chat GPT













