Recubrimientos funcionales con potencial aplicación en bio-implantes óseos
Las personas mayores de 65 años tienen un alto riesgo de desarrollar enfermedades degenerativas del disco intervertebral, artrosis y baja densidad ósea. En México, las personas de 60 años y más constituyen el 12% de la población total, equivalente a 15 millones [1]. Datos del Centro Nacional de Programas Preventivos y Control de Enfermedades (Cenaprece) indican que en México una de cada 12 mujeres y uno de cada 20 hombres mayores de 50 años sufrirán una fractura de cadera en lo que les resta de vida [2, 3], además del aumento de las lesiones en el deporte y los accidentes viales (301,678 casos en 2022) que necesitan implantes ortopédicos [4, 5], explicando así su amplia demanda. En años recientes, el estudio de los biomateriales para implantes se ha centrado en la construcción de estructuras degradables en un tiempo controlado que permita la integración con el tejido humano; se busca que éste sustituya al implante cuando se degrade (Figura 1) [6]. Por ello, los biomateriales degradables para la reparación ósea son de gran interés, ya que se pudiera ahorrar el trauma (dolor) y el costo de una segunda cirugía para la extracción del implante [7].
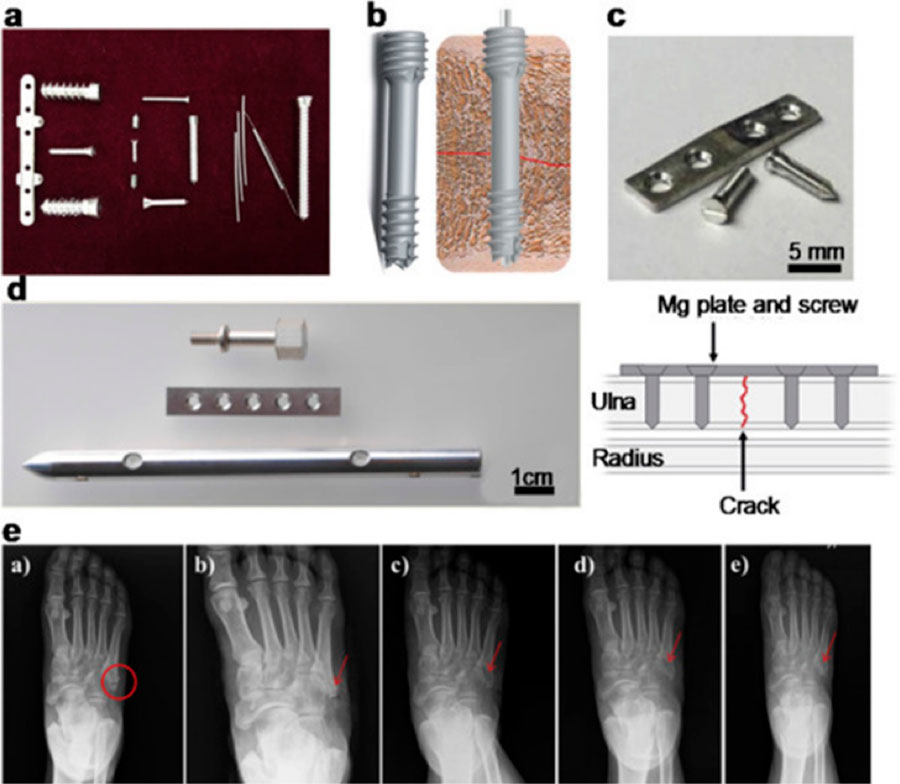
Un elemento químico como el magnesio (Mg) y sus aleaciones, tiene el potencial de emplearse como implantes bio-compatibles, osteo-conductores y portadores de carga degradables. El Mg es un metal ligero con propiedades mecánicas similares al hueso cortical humano. Además, sus productos de degradación (corrosión) no son tóxicos y pueden ser absorbidos en su totalidad por la sangre, participar en las funciones biológicas y desecharse a través de la orina [8]. Sin embargo, una de sus principales desventajas es su alta velocidad de corrosión en ambientes ricos en iones cloro (Cl–), que son de los principales constituyentes del fluido corporal. Esta rapidez ocasiona que el implante se degrade parcial o totalmente antes de la recuperación completa de las fracturas óseas. Durante el proceso de corrosión también se libera gas hidrógeno (H2), que puede dañar el tejido al incrementar el pH del entorno donde se coloque el implante, lo cual es una preocupación en las aplicaciones médicas [9].
En un metal, existen dos formas de mejorar la resistencia a la corrosión; la primera es modificando su estructura interna y la segunda realizando alteraciones superficiales que sirvan de barrera. En el cambio estructural, se adapta la composición, incluido el tamaño de grano, optimizando los métodos de fabricación y las materias primas adecuadas. En la rectificación superficial, se lleva a cabo una serie de tratamientos químicos o se utilizan recubrimientos con capas protectoras de cerámica o polímeros. Aquí es donde interviene la hidroxiapatita (HAp) cuya fórmula química es Ca5(PO4)3(OH), la cual es un fosfato de calcio considerado un material cerámico. Por sí solo, no sirve como soporte estructural ni para someterse a grandes esfuerzos por sus bajas propiedades mecánicas; sin embargo, utilizándolo como recubrimiento en sustratos de titanio (Ti) muestra bioactividad y biocompatibilidad, dado que la HAp deficiente en calcio es el principal componente mineral del hueso [10].
La combinación de soporte/recubrimiento del Mg/HAp se sitúa como una de las mejores combinaciones dado que la HAp disminuye la producción de H2, reduciendo los sitios activos a la corrosión superficial [11]. Además, los iones de magnesio (Mg2+) tienen flexibilidad para unirse a los fosfatos del cuerpo, lo que influye en la mineralización del tejido óseo mediante la formación de más capas de HAp y así regenerar el hueso.
Tomando en cuenta que el Mg está rodeado de los fluidos corporales, en el laboratorio de materiales funcionales del departamento de Física Aplicada del Centro de Investigación y de Estudios Avanzados del IPN unidad Mérida (CINVESTAV) se trabaja en el desarrollo y síntesis de materiales bio-compatibles para su uso como recubrimientos de posibles implantes temporales. En este caso, hemos diseñado en conjunto con el Centro de Biomateriales (BIOMAT) de la Universidad de La Habana en Cuba un recubrimiento protector de HAp para sustratos de magnesio puro.
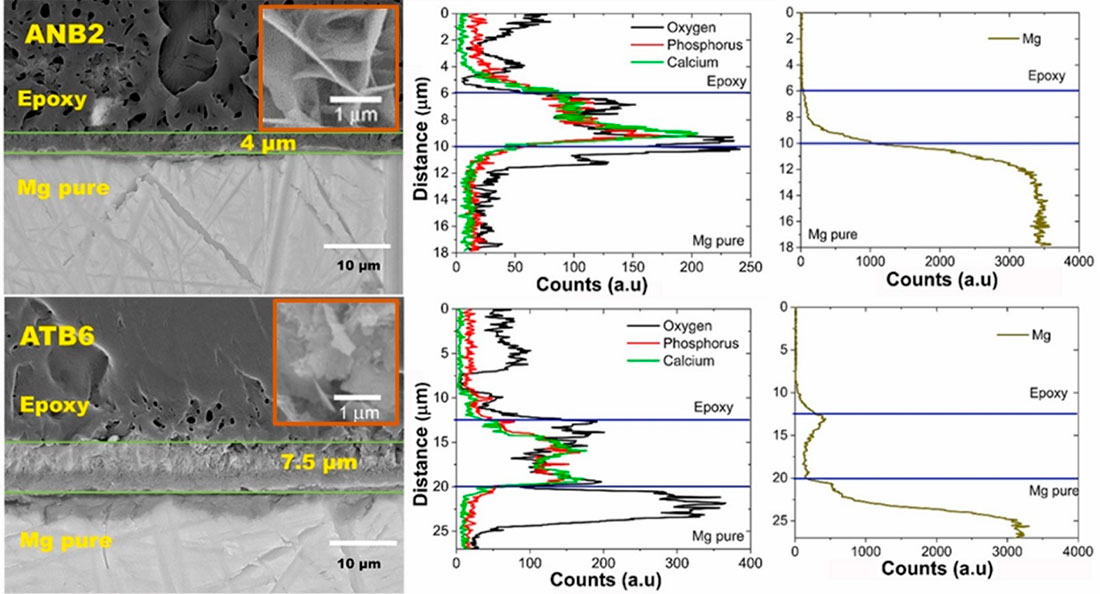
Para la formación del recubrimiento de HAp empleamos el método biomimético, que consiste en sumergir un metal sin suministro de corriente en una solución fisiológica durante un lapso determinado. Con el tiempo, se producen reacciones químicas en la interfase que promueven la nucleación de los fosfatos de calcio (Ca3(PO4)2). En este método se imitan los procesos de mineralización del hueso, la temperatura corporal y el pH del entorno. La solución fisiológica utilizada es SCS (supersaturated calcification solution, por sus siglas en inglés), la cual es una modificación de la solución SBF (Simulated Body Fluid). SCS al tener una mayor concentración de iones, acelera el proceso de formación de HAp en la superficie del Mg. Como se señala en la Figura 2, los resultados fueron exitosos; se obtuvieron nano-placas de HAp de aproximadamente 20 µm de espesor y la técnica de SEM-EDS mostró contenido principal de HAp. Las técnicas de espectroscopia de fotoelectrones de rayos X (XPS), la difracción de rayos X (DRX), la espectroscopia Raman y el infrarrojo por transformada de Fourier (FTIR) para el análisis cuantitativo local y determinación estructural mostraron la obtención de HAp con un porcentaje de Ca, lo que es adecuado en el sentido de la bio-compatibilidad, ya que el hueso humano contiene HAp con un 4-6% de carbonato en peso, llamado Dahllita. Los espesores obtenidos fueron de 4 a 7.5 µm, lo que llevó a lograr valores de OCP cercanos a -1.47 V, indicando menores sitios activos para la corrosión. Por lo tanto, estos resultados abren la puerta a la reducción de costos y traumas en las operaciones y la degradación temprana de los implantes temporales en el cuerpo humano. Para conocer en detalle la metodología y los resultados sugerimos revisar el artículo publicado en la revista Ceramics International [12].
Referencias
- www.inegi.org.mx/contenidos/saladeprensa/aproposito/2021/EAP_ADULMAYOR_21.pdf
- www.cenaprece.salud.gob.mx/programas/interior/adulto/descargas/pdf/OGC_CENAPRECE_Digital_100217.pdf
- www.gob.mx/profeco/documentos/osteoporosis-no-descuides-tu-salud-osea?state=published
- Prakasam, M., et al., Biodegradable materials and metallic implants—a review. Journal of functional biomaterials, 2017. 8(4): p. 44.
- www.inegi.org.mx/temas/accidentes/
- Yang, Y., He, C., Dianyu, E., Yang, W., Qi, F., Xie, D., … & Shuai, C. (2020). Mg bone implant: Features, developments and perspectives. Materials & Design, 185, 108259.
- Hernández-Montes, V., C.P. Betancur-Henao, and J.F. Santa-Marín, Titanium dioxide coatings on magnesium alloys for biomaterials: A review. Dyna, 2017. 84(200): p. 261-270.
- Staiger, M.P., et al., Magnesium and its alloys as orthopedic biomaterials: a review. Biomaterials, 2006. 27(9): p. 1728-1734.
- Hornberger, H., S. Virtanen, and A. Boccaccini, Biomedical coatings on magnesium alloys–a review. Acta biomaterialia, 2012. 8(7): p. 2442-2455.
- Bermúdez-Reyes, B., et al., Cyclic polarization and immersion corrosion test on HA/ZrO2/316LSS for application on orthopedics prosthesis. International Journal of Electrochemical Science, 2012. 7: p. 2028-2035.
- Lu, W., et al., Microstructure, corrosion resistance and biocompatibility of biomimetic HA-based Ca-P coatings on ZK60 magnesium alloy. Int. J. Electrochem. Sci, 2012. 7(12): p. 12668-12679.
- Hernandez, L., Gonzalez, J. E., Barranco, V., Veranes-Pantoja, Y., Galván, J. C., & Gattorno, G. R. (2022). Biomimetic hydroxyapatite (HAp) coatings on pure Mg and their physiological corrosion behavior. Ceramics International, 48(1), 1208-1222.