Definiendo al cáncer
Las células que forman un organismo están cuidadosamente programadas para cumplir funciones específicas en los diversos órganos y tejidos. Este programa contiene información que define su fenotipo (ver glosario donde se definen todos los términos en cursivas) y sus interacciones con otras células del organismo y con su medio ambiente. El programa en cuestión está orquestado por la expresión ordenada de múltiples genes que le indican a la célula, entre otras cosas, cuándo dividirse o cuándo dejar de hacerlo. De manera particular, aquellos genes cuyo incremento en sus niveles de expresión favorecen el surgimiento del cáncer se les conoce como oncogenes, mientras que aquellos genes donde la inhibición de su expresión favorece la carcinogénesis se les designa genes supresores de tumor.
Cuando las células acumulan alteraciones en la información contenida en los genes (mutaciones) cuyos productos proteicos regulan procesos como la proliferación, la diferenciación, la muerte celular o la capacidad de una célula para migrar o invadir otros tejidos, pueden convertirse en células iniciadoras de tumores (CIT). Las CIT pueden proliferar descontroladamente, dejar de ejercer sus funciones y no obedecer las señales de muerte que el organismo genera cuando su tiempo de vida ha finalizado o se detecta algún daño o alteración. De modo que, crecen como un sistema autónomo, pero al mismo tiempo integrado al organismo (lo que reconocemos como un tumor), para después invadirlo colapsando al órgano que las contiene e invadiendo otros órganos en un proceso que se conoce como metástasis.
La mayoría de los cánceres (90%) son de origen epitelial, es decir, se originan en los epitelios o endotelios, que son capas de células que recubren los órganos o sus cavidades. El porcentaje restante incluye cánceres originados en el tejido conectivo (sarcomas); cánceres originados en los linajes celulares sanguíneos (leucemias); y tumores neuro-ectodérmicos (gliomas, schwannomas y meduloblastomas).
Aunque mucho se ha teorizado sobre el origen del cáncer, aún no se tiene un consenso que recapitule o unifique las diferentes hipótesis existentes. En este artículo nos centraremos en una de las líneas de pensamiento más atractivas en la actualidad, en la que el eje fundamental es la adquisición de características de troncalidad por parte de las células que inician un tumor.
Las células troncales, entidades que pueden autorreplicarse y diferenciarse
Actualmente sabemos que los tejidos de los seres vivos están en constante renovación; los antiguos dogmas como la sentencia: “las células del cerebro no se regeneran”, han sido redefinidos a la luz de nuevos conocimientos, estableciéndose un nuevo paradigma en el cual, de manera silenciosa, las células envejecidas o dañadas son reemplazadas por células jóvenes que mantienen la funcionalidad de un órgano. Salvo condiciones excepcionales, una nueva célula no se genera por división de otra ya diferenciada, debido quizás a que las células guardan evidencia de su envejecimiento. La tarea de renovar las poblaciones celulares está reservada a las denominadas células troncales (CT, del inglés stem cells). Las CT se encuentran en todos los tejidos y poseen características particulares que les permiten proliferar y generar una progenie altamente especializada (diferenciada), pero, al mismo tiempo, mantienen sus características fundamentales.
Un ejemplo muy ilustrativo ocurre en el hígado, donde un nicho de células troncales, denominadas históricamente células ovales, se localiza flanqueando los conductos biliares intrahepáticos o conductos de Hering. Ante estímulos dañinos que producen inflamación, como el uso excesivo de medicamentos o el consumo de alcohol, las células ovales pueden diferenciarse hacia células biliares (colangiocitos) o hepatocitos, dos tipos celulares esenciales para el hígado, sin que el nicho de células ovales se agote, contribuyendo a conservar la integridad del órgano.
Otro ejemplo puede observarse en el cerebro adulto, en donde las neuronas bien diferenciadas no pueden dividirse, pero la génesis de nuevas neuronas que reemplazan a aquellas que deben ser sustituidas por haber experimentado algún daño o por el cumplimiento de su ciclo vital, se lleva a cabo en zonas específicas de este órgano (el hipocampo y la zona subventricular) a partir de células precursoras que se encuentran agrupadas en sitios específicos (nichos), de donde son reclutadas gracias a señales específicas que se originan en los sitios en donde se han perdido neuronas.
Las CT poseen tres características fundamentales: 1) capacidad de diferenciación, lo que significa que cambios en la expresión génica inducen su conversión en una célula especializada; 2) capacidad de autorrenovación, lo que implica que al dividirse pueden generar una célula hija diferenciada y otra que mantiene las propiedades troncales, conservándose así el nicho de células no diferenciadas; y 3) susceptibilidad de ser reguladas por los mecanismos de control de la renovación tisular (homeostasis tisular), lo cual significa que, ante señales específicas, inician su propia proliferación y diferenciación para mantener un tejido funcional.
Las células troncales, son en cierto sentido, inmortales. Pueden autorrenovarse y poseen una gran capacidad de diferenciación. El enigmático atractivo de dichas células se pone de manifiesto al explicar su relación con la génesis de una de las enfermedades que más aquejan a nuestra civilización, el cáncer. Entonces ¿cuál es la relación entre las células troncales y el cáncer?
Las células troncales y el origen del cáncer
En 1855 Rudolf Virchow sugirió que las células cancerosas derivan de otras células del organismo, años más tarde Julius Cohnheim, quien había sido discípulo de Virchow, propuso que el cáncer es resultado de la reactivación de tejido embrionario remanente en los órganos, cuyo desarrollo se encuentra arrestado. Una reformulación actual de esa idea es que las CIT derivan de CT, idea que ha sido plasmada en la “teoría de las células troncales de cáncer” (CSC, por sus siglas en inglés, cancer stem cells,). Esa teoría sugiere que la CT pueden ser generadoras de la enfermedad. De acuerdo con esta teoría, las CT normales residentes en cada órgano acumulan mutaciones inducidas por factores ambientales como la alimentación, la exposición a ciertos agentes químicos o a radiación. Si estas mutaciones afectan genes supresores de tumor u oncogenes, entonces dichas células adquieren propiedades tumorigénicas ignorando las señales de control de la renovación tisular, escapando del control proliferativo y adquiriendo la capacidad de evadir los mecanismos de muerte celular programada (Figura 1).
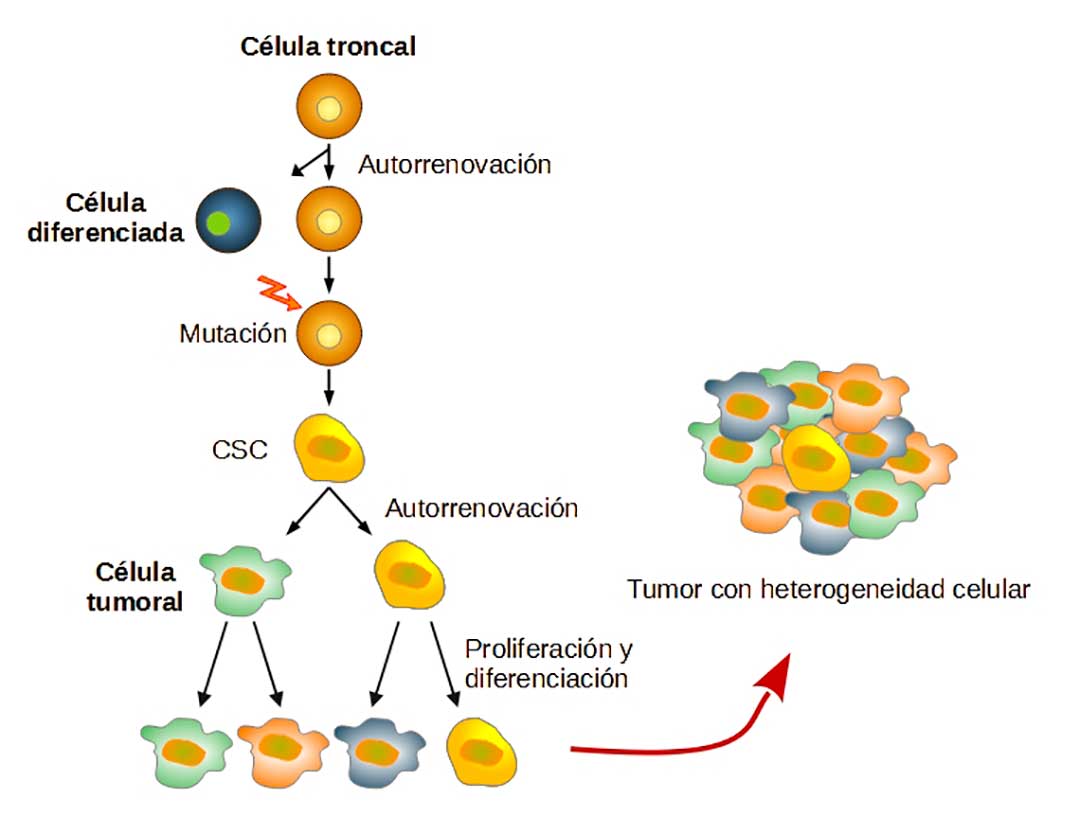
Uno de los principios fundamentales de los cuales deriva esta teoría, se basa en que una de las características esenciales de un tumor es poseer heterogeneidad celular, es decir, células tumorales con diferentes grados de diferenciación y también CSC (no diferenciadas). Así, de todas las células que conforman un tumor, sólo un pequeño número -con características específicas- posee la capacidad para generar un nuevo tumor en toda su complejidad y diversidad. Esta afirmación es el resultado de diversos trabajos experimentales. En los años 90, John Dick y colaboradores, estudiando los mecanismos que subyacen al surgimiento de cierto tipo de leucemia, aislaron las células sanguíneas de un paciente y las agruparon de acuerdo con sus distintos fenotipos, los cuales estaban definidos por la expresión de ciertas proteínas presentes en la membrana celular (marcadores celulares, CD´s del inglés cummulus of differentiation) característicos de cada subpoblación. Células con cada uno de los fenotipos fueron implantadas en ratones cuyo sistema inmune era deficiente con el fin de observar su capacidad tumorigénica. Sólo aquellas que presentaban un fenotipo específico: CD34positivo/CD38negativo, fueron capaces de inducir la enfermedad en los ratones y generar toda la diversidad celular que presentan los pacientes, de una forma jerárquica, similar al proceso de diferenciación de las células sanguíneas (hematopoyesis) a partir de un sólo subtipo celular. Estas células comprendían menos del 4% del tumor total y poseían propiedades troncales.
El postulado anterior también ha sido analizado en el desarrollo de tumores sólidos. Uno de los estudios iniciales fue el realizado por el grupo de Michael Clark en 2003 en tumores epiteliales de glándula mamaria. De manera análoga al estudio anterior, se aislaron células individuales con los diferentes fenotipos presentes en distintos tumores. Células individuales de cada uno de los fenotipos fueron implantadas por separado en ratones inmunocomprometidos. Las únicas células capaces de inducir la formación de un tumor fueron las que presentaban el fenotipo CD44positivo/CD24negativo (sólo un 2% del total). Adicionalmente, en el tumor producido por esas células troncales podía observarse toda la diversidad fenotípica encontrada en el tumor original. De manera paralela, se realizaron experimentos utilizando tumores cerebrales. En estos estudios se describió que sólo las células con un fenotipo CD133positivo podían desarrollar dichos tumores al ser implantadas en ratones.
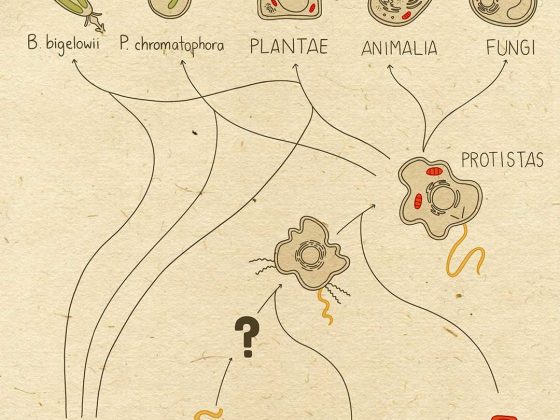
Los estudios mencionados, lograron obtener las primeras evidencias experimentales que sustentan la teoría de las CSC. Con el paso del tiempo, se ha logrado identificar CIT en diversos tipos de cánceres (Figura 2).

Una teoría alternativa que explica el origen de las CSC, propone que un tumor se origina por la acumulación de mutaciones en oncogenes o en genes supresores de tumores en cualquier célula de un órgano, incluyendo células ya diferenciadas, dando como resultado la pérdida del control del ciclo celular, es decir del control proliferación/muerte. Este proceso se conoce como “desdiferenciación” y conduce a las células diferenciadas a adquirir características troncales. Algunos autores han propuesto que la desdiferenciación de células especializadas representa un retorno al fenotipo que poseían durante el desarrollo embrionario. Curiosamente estas células cumplen las condiciones para ser consideradas CSC. Otras teorías, en las que no profundizaremos dada la naturaleza de este texto, sugieren que ambos orígenes de las CSC no son mutualmente excluyentes, pues dada la heterogeneidad de las células de cáncer y su gran plasticidad, el cáncer puede ser visto como la acción conjunta de distintas células con diferentes mutaciones dentro de la misma población, lo cual sugiere que las CSC pueden tener múltiples orígenes debido a las presiones de selección a las que un organismo se somete.
Podemos resumir las características de las CSC de la siguiente manera: 1) son células capaces de inducir un tumor si se le trasplanta en animales de experimentación susceptibles; 2) los tumores inducidos por CSC presentan heterogeneidad fenotípica similar a la del tumor original, poniendo en evidencia que se diferencian a medida que el tumor se establece; 3) los tumores generados por las CSC poseen una población de células con el fenotipo de las CIT originales; 4) las CSC no experimentan senescencia si se les cultiva indefinidamente. Estudios detallados han establecido que las CSC presentan, además, mecanismos que las hacen resistentes a fármacos quimioterapéuticos y les permiten evadir la inmunidad antitumoral.
Independientemente de su origen, el concepto de CSC condensa diversas propiedades de las CIT y esto ha permitido elaborar hipótesis que han llevado a la realización de nuevos proyectos de investigación encaminados a entender cabalmente el cáncer y proponer alternativas innovadoras de tratamiento.
Una breve reflexión final
El cáncer es una de las principales causas de muerte en el mundo; en 2020 causó casi 10 millones de muertes (GLOBOCAN, 2020), por lo que constituye uno de los problemas principales que la humanidad encara en materia de salud pública y bienestar social. Esto ha conducido a que, desde hace varios años, el cáncer sea sujeto de una gran cantidad de estudios clínicos y de ciencia básica.
Develar la identidad y establecer con claridad las características de las células que pueden iniciar un proceso canceroso es fundamental para entender los principios de la homeostasis o equilibrio de los tejidos, pero también abre posibilidades al desarrollo de nuevas terapias.
Desde el punto de vista biológico, el concepto de CSC es muy atractivo y representa un punto de referencia para el entendimiento específico de las propiedades de una célula tumoral. No hay que olvidar que las características de las CSC han sido seleccionadas por la evolución. Resulta entonces paradójico cómo la unidad de mantenimiento y renovación que asegura la función de un órgano a través de la vida, bajo ciertas circunstancias pueda colapsar al sistema. Es sin duda asunto para la reflexión y, sobre todo, para la experimentación.
Lecturas para profundizar:
Weinberg RA. The biology of cancer (2014) Garland Science, NY, EUA.
Hanahan, D., & Weinberg, R. A. (2011). Hallmarks of cancer: the next generation. Cell, 144(5), 646–674. https://doi.org/10.1016/j.cell.2011.02.013
Pardal, R., Clarke, M. F., & Morrison, S. J. (2003). Applying the principles of stem-cell biology to cancer. Nature Reviews Cancer, 3(12), Article 12. https://doi.org/10.1038/nrc1232
Hanahan, D. Hallmarks of Cancer: New Dimensions. Cancer Discovery 12: 31-46, 2022. doi: 10.1158/2159-8290.CD-21-1059
Global Cancer Observatory (GLOBOCAN): https://gco.iarc.fr/en
Glosario:
| Fenotipo | Cualquier característica observable de un organismo. Por ejemplo, la estatura de una persona, el color de los ojos de una mosca de fruta, la expresión de una proteína en la membrana de una célula, etc. |
| Genotipo | Información genética de un organismo. Conjunto de genes, expresados o no, que se encuentran en la secuencia de DNA. |
| Mutación | Variación en la secuencia de DNA de un organismo y, por tanto, en la información codificada en los genes o presente en las secuencias reguladoras de cada gen. |
| Oncogén | Gen que, al sufrir una mutación que incrementa su expresión o aumenta la actividad de la proteína para la cual codifica, favorece la carcinogénesis. Ejemplos: KRAS, BRAF, PIK3CA, etc |
| Gen supresor de tumores | Gen que, al sufrir una mutación de pérdida o disminución de su expresión, atenuando la actividad de la proteína para la cual codifica, favorece la carcinogénesis. Ejemplos: Rb, p53, BRCA2, etc. |
| Metástasis | Proceso por el que las células transformadas provenientes de un tumor primario se propagan a sitios donde pueden generar tumores secundarios. |
| Troncalidad | Capacidad que poseen las células en diferenciarse en distintos tipos celulares. |
| Células troncales | Aquellas que poseen troncalidad. |
| Célula diferenciada | Célula con un fenotipo definido. Por ejemplo, los miocitos del músculo, los hepatocitos del hígado, etc. |
| Diferenciación celular | Proceso mediante el cual las células adquieren un fenotipo distinto, generalmente más especializado, a partir de células precursoras. La base molecular de la diferenciación celular es un cambio en su expresión de genes. |
| Nicho de células troncales | Sitio anatómico con características celulares físicas y químicas definidas que favorece la generación o mantenimiento, la diferenciación y el funcionamiento de las células troncales. |
| Inflamación | Respuesta fisiológica de los organismos multicelulares a alteraciones de la homeostasis, tales como daño al tejido, infecciones por microorganismos o senescencia. La inflamación está orquestada dada por células especializadas pertenecientes al sistema inmune. |
| Leucemia | Tipo de cáncer de la sangre que afecta a las células de la médula ósea y altera el número y función de células inmunes en la circulación. |
| Control de la homeóstasis tisular | Conjunto de procesos que permiten la viabilidad y funcionalidad de un tejido, como la proliferación celular, la diferenciación y la muerte. Estos procesos están regulados por las interacciones con el entorno y se activan o se apagan en respuesta a señales específicas. |
| Marcadores celulares
(Cluster of differentiation, CD) |
Proteínas (generalmente presentes en la membrana celular), que permiten la identificación de linajes o tipos celulares específicos. Algunas de estas proteínas se encuentran presentes solo en ciertos tipos celulares o en células en condiciones particulares. |
| Senescencia replicativa | Proceso que se produce por alteraciones que ocurren por múltiples ciclos de duplicación de una célula. Se caracteriza por el acortamiento de los telómeros, el arresto del ciclo celular, adquisión de un fenotipo secretor de moléculas proinflamatorias y cambios en el metabolismo celular, entre otras alteraciones ocasionadas por la acumulación de mutaciones en el DNA de una célula. |