La etimología de la palabra átomo nos dice que, en latín, atŏmo significa la menor porción de un conjunto que al aislarla de éste mantiene sus mismas propiedades. Por ejemplo, si se divide un átomo de Hidrógeno en el protón y el electrón que lo constituyen, estas partículas por separado no conservan las propiedades del átomo. Así, los atŏmos que conocemos aparecen representados en la Tabla Periódica de los elementos químicos. Una pregunta que existe desde que Dmitri Mendeléyev publicó en 1869 la primera versión de esa tabla, es cuál es el número máximo posible de atŏmos que pueden existir en la naturaleza o ser creados por el hombre. Aquí intentaremos dar una respuesta acerca de esta pregunta, y en ella conoceremos sobre un número “mágico” de la Física. Por otra parte, según el griego antiguo, la palabra ἄτομο quiere decir indivisible. La búsqueda de los ἄτομος o ladrillos básicos de la naturaleza también ha ocupado a la ciencia desde que los griegos introdujeron la idea del atomismo 2500 años atrás. Nuestra intención aquí es describir la tabla periódica de esos ladrillos. La temática de los atŏmos y los ἄτομος no está cerrada. Veremos algunos resultados recientes que lanzan luz sobre algunas cuestiones importantes para saber de qué y cómo está hecho el universo.
ἄτομος : Los indivisibles
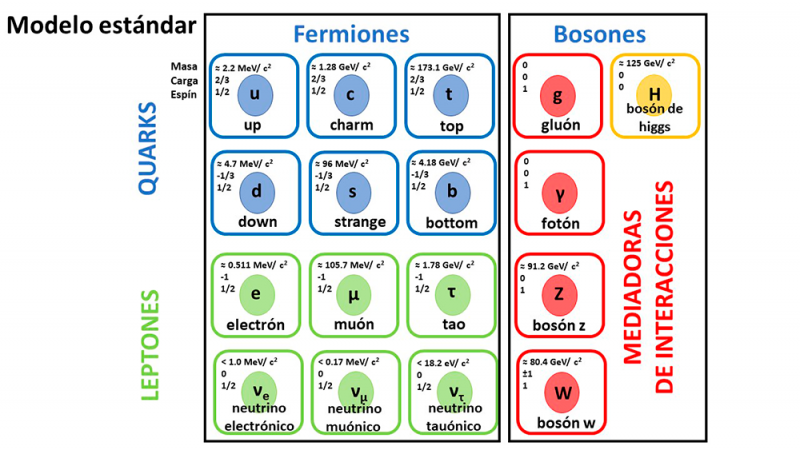
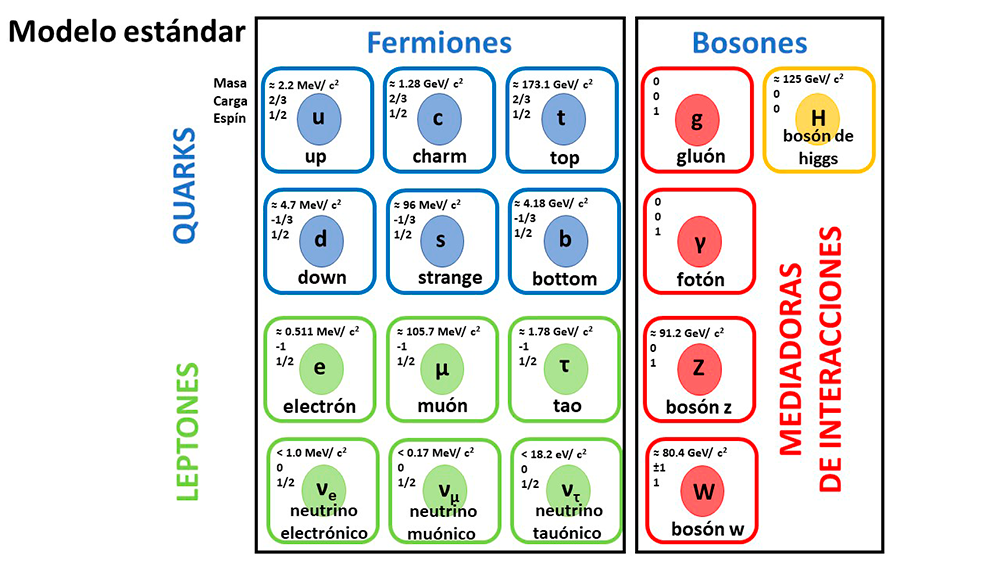
En la actualidad, técnicas modernas de análisis y herramientas poderosas fisicomatemáticas han hecho posible “observar” la naturaleza hasta distancias de 10-18 m, es decir, la millonésima parte de una billonésima de un metro. Ese es el límite experimental actual, un límite técnico, aunque no fundamental. Ese valor es mil veces menor que un femtómetro o fermi (1fm = 10-15 m), tamaño aproximado del núcleo de un átomo. Debido a ese límite experimental, el electrón se revela como una partícula fundamental, sin estructura interna, indivisible: uno de los ἄτομος. Se ha demostrado que el neutrón y el protón, las constituyentes nucleares, se conforman por quarks, partículas a su vez sin estructura interna hasta el mismo límite experimental de 10-18m. El modelo estándar de la Física de Partículas (MEFP) ha establecido la “Tabla periódica” de los ἄτομος (Fig. 1).
Según ese modelo, respaldado en gran medida por las observaciones experimentales y aceptado por la mayoría de los especialistas en estos temas, los quarks no existen aislados, sino que interactúan fuertemente entre sí y se agrupan para ser los constituyentes de un grupo de partículas llamadas hadrones, entre los cuales clasifican también los nucleones. Los hadrones, en dependencia de sus masas, se clasifican a su vez en dos grandes grupos, mesones (aquellas con masas medianas formados por dos quarks) y bariones (más pesadas, con tres quarks). Estos últimos a su vez se ordenan en nucleones (protones y neutrones) e hiperones.
Los físicos a veces usan nombres curiosos para denominar a las partículas, como los de los seis quarks: up (u, arriba), down (d, abajo), charm (c, encanto), strange (s, extraño), top (t, cima) y bottom (b, fondo). Generalmente los quarks se unen en grupos de dos o tres. Por ejemplo, el protón está formado por dos quarks up y down y el neutrón por uno up y dos down. El modelo estándar no cuestiona la posible existencia de grupos de más quarks, que formarían lo que se conoce como hadrones exóticos. El pasado mes de julio, científicos del Gran Colisionador de Hadrones (LHC, Large Hadron Collider) del Centro Europeo de Investigaciones Nucleares (CERN), un acelerador de partículas de más de 27 Km de longitud ubicado a 100 metros de profundidad debajo de la frontera entre Francia y Suiza, anunciaron en una Conferencia Internacional de Física de Altas Energías celebrada en Boloña, Italia, el descubrimiento de un pentaquark y dos tetraquarks, con cinco y cuatro quarks respectivamente (LHCb Collab. 2022 arXiv:2206:15233). Estas partículas exóticas fueron predichas en los años 1960s por Murray Gell-Mann y George Zweig cuando, por separado, propusieron el modelo de quarks. El primero de estos científicos fue quien acuñó el término “quark”, tomándolo de la frase “three quarks for Muster Mark” de la novela Finnegan´s Wake del escritor irlandés James Joyce, donde “quark” es una onomatopeya que representa el graznido de una gaviota, es decir, una palabra sin mucho sentido. Además, el número tres del texto de Joyce encajaba con el hecho de que los protones y neutrones están formados por tres quarks.
Por otra parte, los electrones, junto con los neutrinos y los muones, constituyen otro grupo de partículas fundamentales, llamadas leptones (masas relativamente pequeñas). Para cada partícula existe una antipartícula. En general, partículas y antipartículas difieren principalmente en el signo de su carga eléctrica (si la partícula es neutra eléctricamente, su antipartícula será ella misma). Por ejemplo, la antipartícula del electrón es el positrón. Si una partícula se encuentra con su antipartícula ambas desaparecen, y surge un destello de luz que recupera las energías que ambas portaban antes de la colisión.
Los quarks y los leptones son los “átomos” de la actualidad, según la definición griega. Ambos constituyen las partículas fundamentales, al ser “indivisibles” con ayuda de la tecnología actual. Todos ellos son fermiones, con una propiedad intrínseca llamada espín y un valor fraccionario igual a media unidad. Obedecen las leyes de la Estadística Cuántica de Fermi-Dirac. El Principio de Exclusión de Pauli limita la cantidad de fermiones que pueden ocupar un estado energético.
El Modelo Estándar establece también que otro grupo de partículas fundamentales son aquellas involucradas en las principales interacciones: la electromagnética, la fuerte, la débil y la gravitatoria. Todas ellas son Bosones, con espín unitario o nulo, que obedecen leyes de otra Estadística Cuántica, la de Bose-Einstein. Muchos bosones pueden ocupar un mismo estado energético formando lo que se conoce como el Condensado de Bose-Einstein.
El ejemplo más conocido de partícula mediadora es el fotón. Los haces luminosos están formados por fotones. Los fotones son intercambiados entre partículas cargadas durante la interacción electromagnética, aquella que mantiene los electrones orbitando alrededor de los núcleos en los átomos y es responsable de la generación de la energía que ilumina nuestros hogares, y que se postuló para explicar el hecho de que los protones de los núcleos atómicos, partículas eléctricas con carga positiva, se mantuviesen allí pese a su repulsión electromagnética junto a sus hermanos sin carga eléctrica, los neutrones. Este fenómeno sólo funciona dentro de los núcleos atómicos, en cuyo límite se apaga para que la fuerza electromagnética mantenga el equilibrio entre los núcleos positivos y los electrones con carga negativa de los átomos. El mecanismo que rige la interacción fuerte solamente se explicó al descubrirse que los constituyentes básicos de los nucleones son los quarks. La fuerza entre los quarks se transmite por partículas llamadas gluones (del inglés glue, que significa pegamento). La interacción débil se constató al entenderse cómo las partículas beta (electrones y positrones) son producidas durante los mecanismos de transmutación de algunos núcleos atómicos en otros durante determinados procesos de desintegración radiactiva, parcialmente responsables de que el Sol brille. Esta fuerza permite a los protones de los núcleos transformarse en neutrones y viceversa. La interacción se explica asignando a todos los quarks y leptones una carga denominada débil, y considerando partículas virtuales que son intercambiadas durante sus interacciones. Éstas se denominan bosones, y se conocen tres tipos: W+, W– y Z0.
El que los bosones de la fuerza débil tengan masa, mientras que el fotón (otro bosón) no, plantea problemas superados por la hipótesis de la existencia de los campos de Higgs, transmitidos por el bosón del mismo nombre. Al pasar las partículas a través del campo de Higgs, e interactuar con él, se genera una inercia que advertimos como masa, de manera semejante a como percibimos esta magnitud al interactuar un objeto con el campo gravitatorio. En 2012 se anunció su hallazgo en el LHC, también conocido como la “máquina del Big Bang”, donde se han simulado las condiciones inmediatamente posteriores a ese evento para demostrar, por ejemplo, la existencia de partículas hasta ahora sólo hipotéticas, como el bosón de Higgs, considerado el Santo Grial de la Física de Partículas y la Cosmología modernas. Precisamente el premio Nobel de Física de 2013 se otorgó al físico británico de la Universidad de Edimburgo que propuso la existencia del bosón que lleva su apellido, Peter W Higgs, y a Francois Englert, de la Universidad Libre de Bruselas (Bélgica), quien junto con el primero propuso el mecanismo por el que los objetos adquieren su masa en el Universo.
Por último, la gravitación, que mantiene a los planetas girando alrededor del Sol y hace que los frutos que se desprendan de un árbol caigan al suelo y no hacia arriba, y cuya primera teoría fue formulada por Newton a finales del siglo XVII y extendida por Einstein unos doscientos cincuenta años más tarde en la Teoría General de la Relatividad, no juega un papel importante en las escalas que estamos considerando, aunque a muy elevadas energías puede ser dominante, como lo es a escala cósmica. Para entender ese papel se requiere una teoría inexistente aún, una teoría cuántica de la gravitación en la cual la partícula hipotética que mediaría en la interacción entre dos partículas masivas es el gravitón, del cual tampoco hay evidencias experimentales.
Atŏmos y un número mágico: 137
Algunos tipos de quarks se “pegan” para formar protones y neutrones, los que a su vez se unen para formar los núcleos atómicos. Estos se enlazan con electrones para formar los elementos químicos. Actualmente conocemos 118 de estos elementos, teniendo en cuenta a Oganesón, cuyo símbolo es Og y que tiene un número atómico Z=118 (cantidad de protones en su núcleo), como el elemento más pesado sintetizado hasta ahora y oficialmente reconocido por la Unión Internacional de Química Pura y Aplicada (IUPAC por sus siglas en inglés). El nombre de este elemento fue acuñado en honor al físico nuclear ruso de origen armenio Yuri Oganessian, el “Sr. Elemento 118” según la revista New Scientist, quien junto con su equipo ha sintetizado seis nuevos elementos desde el año 2000.
Cuántos otros elementos químicos podrían existir es una pregunta que muchos nos formulamos. Que tiene que existir un límite máximo es una conclusión obvia, si imaginamos al núcleo atómico con Z protones cargados positivamente que pueden repelerse unos a otros debido a la fuerza electrostática (o de Coulomb), que se incrementa con el aumento de la cantidad de protones, haciendo al núcleo inestable por encima de cierto valor de Z. Pero no puede olvidarse que existe una fuerza que compite con la de Coulomb, siendo mucho más intensa que ella. Ésta, con acción limitada al interior del núcleo atómico, caracteriza a la interacción nuclear fuerte, la responsable de mantener dentro de los núcleos a los protones y a sus hermanos sin carga eléctrica, los neutrones. Así, debe mirarse hacia afuera del núcleo, donde la fuerza de Coulomb gobierna su interacción con los electrones con carga negativa del átomo.
Uno de los modelos más sencillos que explica algunas de las propiedades básicas de algunos tipos de átomos es el de Bohr, al cual le podemos llamar semiclásico o semicuántico, porque reúne aspectos de las Físicas Clásica y Cuántica. La teoría atómica de Bohr parte de tres suposiciones ad-hoc (los tres Postulados de Bohr) y de una ley empírica denominada Fórmula de Rydberg, que describe las energías de las líneas espectrales observadas en el espectro de emisión del Hidrógeno (Fig. 2).

Los tres postulados pueden enunciarse así: 1- los electrones del átomo se mueven alrededor del núcleo en órbitas circulares estacionarias (su radio no cambia con el tiempo como predice la Física Clásica para una carga girando que emitiría energía continuamente en forma de radiación). 2- Solo se emite o absorbe radiación luminosa si el electrón pasa de una órbita de mayor a menor energía, o viceversa, respectivamente. 3- En esas órbitas, el momento angular del electrón, igual al producto de su masa, su velocidad y el radio de su órbita, solo puede tomar algunos valores discretos igual a múltiplos enteros de h/2π, donde π=3.1416…. y h=6,6×10-34 J▪s (J = Joule, s=segundo) es la famosa constante de Planck. Nótese que este valor es igual aproximadamente a un número decimal formado por un seis precedido por treinta y tres ceros como parte decimal. El tercer postulado es una regla de cuantización. Este tipo de reglas rigen en el mundo cuántico, microscópico, pero no se manifiestan a escalas macroscópicas debido al valor infinitesimal de la constante h.
Entonces, partiendo de esos supuestos, y usando el principio de conservación de la energía y la ley de Newton para las fuerzas en equilibrio necesarias para mantener al electrón en la órbita, el modelo de Bohr es capaz de predecir las ecuaciones para calcular los radios de las órbitas, así como la velocidad y energía del electrón en cada una de ellas. Esta última es consistente con el resultado de la teoría cuántica. El modelo de Bohr anticipa esas propiedades no solo para el átomo de Hidrógeno, sino para todos aquellos que, al igual que él, poseen un solo electrón (hidrogenoides). Algunos ejemplos de ellos son el Deuterio (que difiere de su isótopo Hidrógeno en que en su núcleo tiene un neutrón además del protón, manteniendo el mismo Z=1); el Helio ionizado (al átomo de He se le “extrae” un electrón, quedando solamente uno orbitando al núcleo con dos protones y dos neutrones y Z=2); el Litio dos veces ionizado (Z=3), etcétera.
Para la velocidad del electrón en la órbita de menor energía (n=1) de ese tipo de átomos el modelo de Bohr predice el resultado
v = Z α c (1)
donde c=299.792,458 kilómetros por segundo es la velocidad de la luz en el vacío, y α » 1/137 es un número denominado constante de estructura fina.
Supongamos que un núcleo con carga Z se “enlaza” con un único electrón para formar un átomo hidrogenoide. De acuerdo con la ecuación (1), ese electrón en el estado de menor energía tendrá una velocidad
v = Z c / 137 (2)
Entonces, para números atómicos Z mayores que 137 ese electrón se movería a una velocidad mayor a c, un resultado obviamente contradictorio ya que la teoría de la relatividad de Einstein nos indica que esa es la máxima velocidad posible. Por ello, el modelo de Bohr predice a 137 como la cantidad máxima posible de elementos químicos.
Un cálculo más realista deberá tener en cuenta aspectos como la distribución real de carga eléctrica en el núcleo y en los electrones de un átomo multielectrónico, las interacciones entre los electrones entre sí y con el núcleo, aspectos relativistas (movimientos de estas partículas a velocidades cercanas a c), entre otros efectos. Teniendo en cuenta algunos de ellos, varios autores han propuesto valores de Z mayores a 137.
En décadas recientes, en promedio, se ha descubierto un nuevo elemento químico cada tres años. Hace cerca de una década eran 112 los elementos químicos conocidos. Hoy son seis más.
La importancia del número 137 va más allá de lo mencionado hasta aquí. La constante de estructura fina, aproximadamente igual a su inverso, aparece en muchas fórmulas de la física atómica y de partículas. Eso se debe a que la constante está involucrada con la fuerza electromagnética que rige la interacción entre partículas cargadas y fotones. Fue introducida en la Física en 1916 por Arnold Sommerfeld para explicar la existencia de desviaciones en las líneas espectrales atómicas de las predicciones hechas por el modelo de Bohr. Por ejemplo, la línea roja del espectro de la Fig. 3 tiene una longitud de onda de 656.3 nm (1nm = 1 nanómetro es la milmillonésima parte de un metro). Pero si se aumenta la resolución del aparato empleado para la medición del espectro, veríamos que en realidad se compone de dos líneas separadas tan solo por alrededor de la cienmilésima parte de un nanómetro, lo que se conoce como la estructura fina del espectro.
En la actualidad, la constante de estructura fina constituye parte considerable de las ecuaciones que rigen el modelo estándar de la Física, teoría que predice las partículas e interacciones fundamentales de la naturaleza. El modelo estándar es consistente con casi todos los resultados experimentales, pero tiene limitaciones para eliminar cuestiones relacionadas con lo que se denomina materia oscura y balance materia-antimateria del universo (por ejemplo, se han detectado más partículas que sus antipartículas). Para la solución de estas discrepancias resulta primordial contar con valores correctos de las constantes físicas fundamentales. La medición más precisa hasta la fecha de la constante de estructura fina se publicó hace dos años (https://www.nature.com/articles/s41586-020-2964-7), reportándose un valor, para su inverso, de 1/α= 137,035999206(11) (los dos dígitos entre paréntesis corresponden a la incertidumbre de los dos anteriores). Esto significa una incertidumbre relativa de 81 partes por trillón.
La constante de estructura fina es, sencillamente, un número sin unidades que no cambia su dimensión, a diferencia de otras constantes físicas cuyos valores varían según se midan en unas unidades u otras (por ejemplo, la constante de Planck tendría un valor de 4,1×10-15 si se expresase en unidades de eV▪s en vez de J▪s como hicimos antes, donde 1 eV = un electronvoltio = 1.6 x10-19 J). El número 137, que es el valor aproximado del inverso de esa constante, constituye una especie de cantidad mágica en la Física, de la que no sabemos con certeza cómo y por qué aparece en la naturaleza.
El tiempo y la investigación científica dirán la última palabra sobre estos temas.