Introducción
A mediados del siglo XIX, un naturalista de origen alemán, llamado Renous, fue arrestado bajo cargos de herejía en la ciudad de San Fernando, al sur de Santiago de Chile; el motivo… su inusual pasatiempo de transformar orugas en bellísimas mariposas. Charles Darwin lo conoció en 1835 y años después relató esta historia en su Diario de viaje en el H.S.M. Beagle (Darwin, 1839). Esto es un ejemplo de cómo lo que hoy damos por sentado, en algún momento fue desconocido, y en casos extremos, objeto de persecución religiosa (Mitra, 2013).
La “Metamorfosis”, derivada de los vocablos griegos (meta-) “cambio” y (morfe-) “forma”; hace referencia a las transformaciones en el plano corporal posterior al desarrollo embrionario (Laudet, 2011), que ocurren durante la transición o transiciones del estadio larvario hacia el estadio adulto. La metamorfosis no solo es consecuencia de variaciones morfológicas, sino también de cambios fisiológicos, bioquímicos, del comportamiento, y a nivel ecológico (—hábitat, presencia de depredadores y abundancia de recursos nutricionales—) (Paris & Laudet, 2008; Mitra, 2013). Sin embargo, a pesar de ser un proceso común para muchos organismos, el conocimiento de las rutas moleculares responsables de la metamorfosis es escaso (Fuchs et al., 2014).
Desarrollo y ciclos de vida
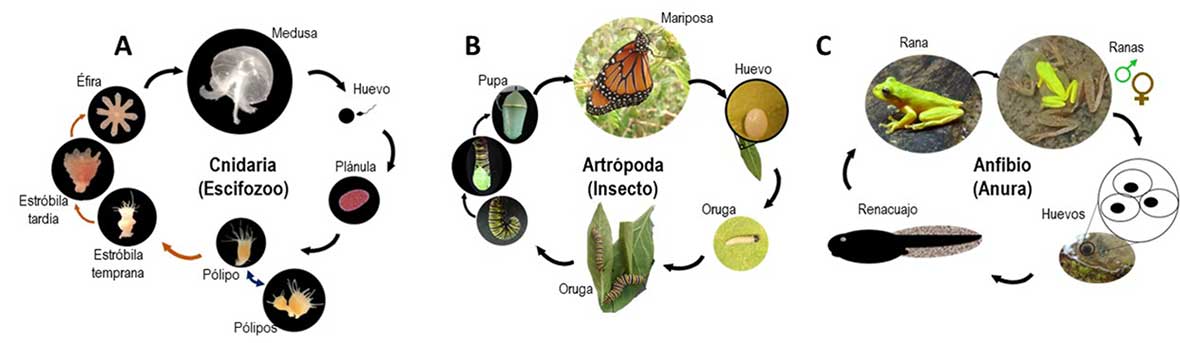
En la mayoría de los taxones animales, un genoma codifica distintas etapas que ocurren a lo largo de la vida de un individuo. Mientras que para algunos organismos (como nosotros) esos cambios morfológicos no son radicales, en otros organismos, como las medusas, las mariposas y anfibios como las ranas (Figura 1), estas transiciones son drásticas ya que el cuerpo de una larva se transforma en uno diferente en la etapa juvenil o adulta. Se pierden estructuras, se producen nuevos órganos e incluso pueden cambiar de hábitats, como es el caso de las ranas y las salamandras, en que los renacuajos completamente acuáticos y que pueden respirar bajo el agua, se vuelven terrestres (Fuchs et al., 2014).
¿Por qué algunos organismos presentan ciclos de vida tan complejos?
El incremento en la complejidad de los ciclos de vida se considera un proceso de adaptación al ambiente, primero, porque se facilita la utilización de recursos específicos para cada etapa, así como la especialización estructural de diferentes órganos para obtener fuentes alternativas de alimento. Y segundo, favorece el crecimiento de la población al reducir la competencia intraespecífica (McMahon & Hayward, 2016).
La metamorfosis es al mismo tiempo una transformación ecológica, dado que la larva y el adulto usualmente no viven en el mismo hábitat; por ejemplo, no comparten los mismos recursos, ni tienen los mismos depredadores. Esto resalta cómo los organismos tienen una estrecha conexión con el ambiente en la mayoría de las especies, y por lo tanto no es de extrañarse que haya señales ambientales con un papel importante en el momento de inducir a las larvas a transformarse en adultos (Laudet, 2011).
¿Cómo se controla el cambio metamórfico?
En los animales, el crecimiento del cuerpo ocurre rápidamente durante los estadios juveniles, y el inicio de la maduración marca el fin del periodo de crecimiento. Es claro que el inicio de la metamorfosis esta influenciado por señales ambientales que solo tienen influencia cuando se alcanza el estadio de desarrollo apropiado. Esto es mediado por sensores en ciertos órganos que transmiten la información ambiental, junto con un sistema que evalúa el estado nutricional y del desarrollo del individuo (Malita & Rewitz, 2021).
Asimismo, estos organismos tienen un punto de control del crecimiento durante el desarrollo juvenil, después del cual se toma una decisión irreversible para regular la transición metamórfica de juvenil a adulto; el inicio de la maduración sexual constituye un punto de no retorno en los animales (Ohhara, Kobayashi & Yamanaka, 2017).
Mecanismos que regulan la metamorfosis
A principios del siglo XX, las primeras evidencias experimentales referentes a la regulación de la metamorfosis se realizaron en anfibios, centrándose en la transformación de renacuajos a ranas. El Dr. J. Frederick Gudernatsch, un anatomista de la Escuela de Medicina de Cornell en Estados Unidos, quien alimentó a renacuajos de Rana temporaria con pequeños trozos de varios órganos de diferentes mamíferos (caballos, cerdos, conejos, etcétera), con la finalidad de estudiar el efecto del extracto de órganos normales y cancerosos sobre el desarrollo de estos anfibios.
El Dr. Gudernatsch encontró que la glándula tiroidea contiene una sustancia que desencadenaba el cambio de renacuajo a rana, siendo éste el primer indicio de que la metamorfosis está controlada por una señal hormonal “Renacuajos que solo han sido alimentados con tiroides, y no otro alimento, desarrollaron patas traseras en 9 días y patas delanteras 2 días después. Lo que normalmente ocurre es que pasan varias semanas entre la aparición de las patas traseras y las delanteras” (página 436 Gudernatsch, J.F. 1914; comentado por Laudet, 2011).
Esto fue confirmado posteriormente por B. M. Allen en 1925, cuando removió la glándula tiroidea de los renacuajos, inhibiendo su metamorfosis (descrito por Brown & Cai, 2007). Julian Huxley (nieto del gran amigo de Charles Darwin Thomas H. Huxley) publicó en 1920 un experimento realizado con Axolotl (o ajolotes) (—una salamandra endémica de México—), a partir de especímenes que se mandaron del Musee d´Anatomie Comparative de París a Oxford, Inglaterra. Usualmente el Axolotl permanece en su morfología larvaria, es decir, en forma de ajolote, pero crece y alcanza la madurez sexual sin transformarse a la morfología de salamandra terrestre (a menos que se le saque del agua accidentalmente); a este fenómeno se le conoce como “neotenia”. Huxley, conociendo los resultados de Gudernatsch alimentó a los ajolotes con tiroides de mamífero lo que ocasionó que espontáneamente se transformaran en Salamandras (Huxley, 1920).
En los insectos, la mayor parte del crecimiento ocurre durante las etapas pre-metamórficas de ninfa o de larva. Para cualquier fondo genético determinado, las señales nutricionales, así como otras variables ambientales como la temperatura, determinan la tasa de crecimiento y la duración de cada estadio de ninfa o larvario (Mirth & Riddiford, 2007). El tamaño es un “punto de control” que garantiza que la larva haya adquirido nutrientes y masa suficientes para completar su desarrollo hasta convertirse en un adulto de tamaño adecuado sin ninguna nutrición adicional (Malita & Rewitz, 2021).
La conservación de la metamorfosis y de sus sistemas de regulación molecular, entre organismos evolutivamente muy distantes como lo son anfibios e insectos, lleva a cuestionarnos sobre el origen de los procesos de metamorfosis. Una posibilidad es que su inicio se encuentre en los cnidarios (medusas, corales y anémonas de mar), los cuales son organismos que se encuentran en la base filogenética de los animales y habitan el planeta desde hace unos 700 millones de años y en algunos de ellos, como las medusas y los hidrozoarios, presentan ciclos de vida complejos (Putnam et al., 2007; Fuchs et al., 2014).
El ciclo de vida de los Medusozoa (Hidrozoo, Cubozoo, Estaurozoos y Escifozoo) consiste en tres estadios de vida bien definidos: plánula larval, pólipo sésil asexual y medusa adulta sexual (Fig. 1A). La transición de pólipo a medusa en la medusa luna (Aurelia aurita), se denomina estrobilación y es un proceso inducido por cambios de temperatura del agua, que desencadena el proceso de metamorfosis (Fuchs et al., 2014; Straehler-Pohl & Jarms, 2022).
Aspectos comparativos de la metamorfosis en anfibios, insectos y medusas.
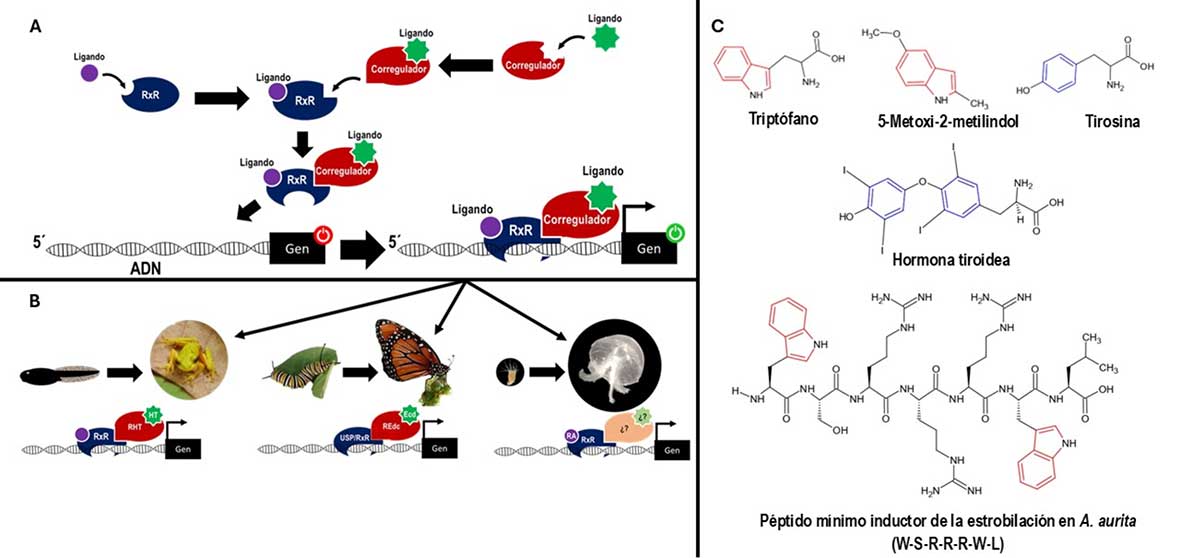
En insectos y anfibios, la transición entre estadios del ciclo de vida está estrechamente regulada por señales neuronales y hormonales, las cuales se integran a nivel de proteínas receptoras de hormonas que se localizan en el núcleo de las células; las mismas proteínas receptoras también se encuentran presentes en las medusas (Fuchs et al., 2014).
Interviniendo en la regulación molecular de la metamorfosis en anfibios, insectos y de las medusas Aurelia aurita, el receptor del ácido retinoico (RxR) forma parte del módulo molecular central que controla el proceso de transición de una etapa juvenil a una adulta (Figura 2). Además, se encontró que el péptido mínimo inductor de la estrobilación de A. aurita contiene un anillo indol (elemento central del aminoácido triptófano), lo cual es un hecho relevante, ya que la hormona tiroidea de vertebrados es un producto de condensación de un aminoácido aromático “tirosina” (Figura 2C). Esto nos invita a hacer la conjetura de que hay principios generales y ligados entre la regulación de la metamorfosis en la medusa A. aurita y de animales más derivados (Fuchs et al., 2014).
Conclusión
La metamorfosis sigue captando la atención de la comunidad científica, debido a que es un proceso muy conservado en diferentes taxones de animales. Este cambio morfológico y fisiológico del plano corporal, ha permitido que los organismos optimicen los recursos de su hábitat, evitando la competencia por recursos entre los estadios larvales y los estadios adultos; además, les ha permitido colonizar nuevos nichos ecológicos con lo cual han podido seguir dispersando a su descendencia. Conocer los mecanismos moleculares regulatorios de la metamorfosis podrá brindarnos una idea de cómo este proceso ha podido evolucionar dentro de muchas ramas del árbol de la vida.
Bibliografía
Aranda, A., & Pascual, A. (2001). Nuclear hormone receptors and gene expression. Physiological reviews, 81(3), 1269-1304.
Brown, D. D., & Cai, L. (2007). Amphibian metamorphosis. Developmental biology, 306(1), 20-33.
Darwin, C. (1839). Journal of Researches Into the Geology and Natural History: Of the Various Countries Visited by HMS Beagle, Under the Command of Cpt. Fitzroy, from 1832 to 1836. London: Henry Colburn, Great Marlborough Street, p 326.
Fuchs, B., Wang, W., Graspeuntner, S., Li, Y., Insua, S., Herbst, E. M., Dirksen, P., Böhm, A. M., Hemmrich, G., Sommer, F., Domazet-Loso, T., Klostermeier, U. C., Anton-Erxleben, F., Rosenstiel, P., Bosch, T. C. G. & Khalturin, K. (2014). Regulation of polyp-to-jellyfish transition in Aurelia aurita. Current Biology, 24(3), 263-273.
Gudernatsch, J. F. (1914) Feeding experiments on tadpoles. II. A further contribution to the knowledge of organs with internal secretion. American Journal of Anatomy. 15, 431-476.
Huxley, J. S. (1920). Metamorphosis of axolotl caused by thyroid-feeding. Nature, 104(2618), 435-435.
Laudet, V. (2011). The origins and evolution of vertebrate metamorphosis. Current Biology, 21(18), R726-R737.
Malita, A., & Rewitz, K. (2021). Interorgan communication in the control of metamorphosis. Current opinion in insect science, 43, 54-62.
McMahon, D. P., & Hayward, A. (2016). Why grow up? A perspective on insect strategies to avoid metamorphosis. Ecological entomology, 41(5), 505-515.
Mirth, C. K., & Riddiford, L. M. (2007). Size assessment and growth control: how adult size is determined in insects. Bioessays, 29(4), 344-355.
Mitra, A. (2013). Cinderella’s new shoes–how and why insects remodel their bodies between life stages. Current science, 1028-1036.
Ohhara, Y., Kobayashi, S., & Yamanaka, N. (2017). Nutrient-dependent endocycling in steroidogenic tissue dictates timing of metamorphosis in Drosophila melanogaster. PLoS genetics, 13(1), e1006583.
Paris, M., & Laudet, V. (2008). The history of a developmental stage: metamorphosis in chordates. genesis, 46(11), 657-672.
Putnam, N. H., Srivastava, M., Hellsten, U., Dirks, B., Chapman, J., Salamov, A., Terry, A., Shapiro, H., Lindquist, E., Kapitonov, V. V., Jurka, J., Genikhovich, G., Grigoriev, I. V., Lucas, S. M., Steele, R. E., Finnerty, J. R., Technau, U., Martindale, M. Q. & Rokhsar, D. S. (2007). Sea anemone genome reveals ancestral eumetazoan gene repertoire and genomic organization. Science, 317(5834), 86-94.
Straehler-Pohl, I., & Jarms, G. (2022). Back to the roots, Part 1—Early life cycle data of Rhopaliophora (Scyphozoa, Cubozoa and Staurozoa). Plankton and Benthos Research, 17(1), 1-33.