El esteviósido es un glucósido diterpenoide que se encuentra en las hojas de la planta stevia rebaudiana Bertoni y presenta diversas propiedades farmacológicas contra patologías como la diabetes mellitus tipo 2 y el síndrome metabólico, en donde la inflamación juega un papel primordial.
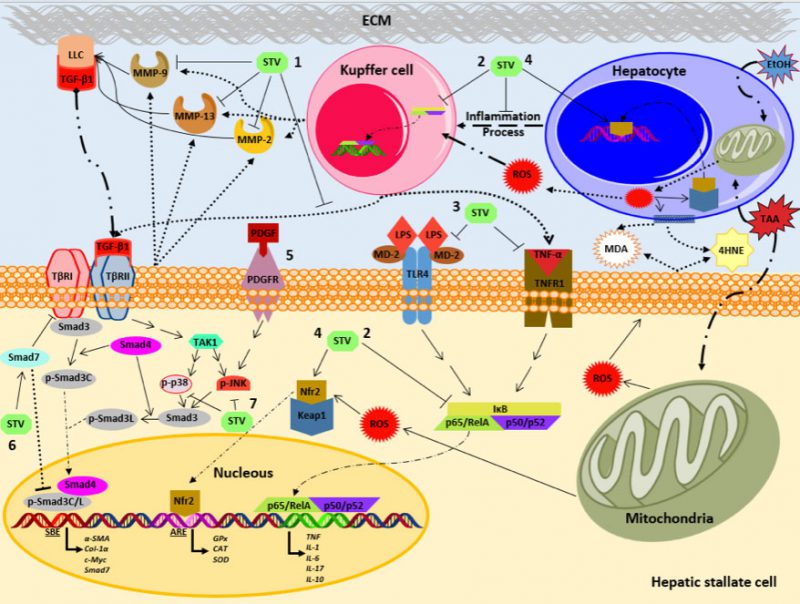
En este proyecto se investigaron las propiedades farmacológicas del esteviósido para prevenir la cirrosis inducida experimentalmente en ratas. Se encontró que el esteviósido puede actuar a diferentes niveles en la lesión hepática inducida con la administración del agente hepatotóxico tioacetamida, modelo que se asemeja a la cirrosis desarrollada en el humano por la ingesta excesiva de etanol. Esto se debe a que el esteviósido previno la colestasis (interrupción del flujo biliar), la necrosis (muerte de células), la fibrosis (desarrollo excesivo de tejido conectivo fibroso), el estrés oxidante (disminución de las defensas antioxidantes intracelulares) y el proceso inflamatorio al actuar como un antioxidante indirecto regulando los niveles del factor nuclear 2 relacionado con el eritroide 2 (Nrf2). Éste regula la expresión inducible de numerosos genes de enzimas destoxificantes y antioxidantes, por lo tanto mantiene los niveles de proteínas antioxidantes y disminuye el estrés oxidante intracelular. Por otro lado, se encontró que el esteviósido es capaz de actuar como un agente inmunomodulador a través de interactuar con el factor nuclear κB (NF-κB), consistente en una familia de factores de transcripción que participan activamente en los procesos de inflamación, inmunidad, proliferación, diferenciación y supervivencia celular. El esteviósido al interactuar con la subunidad p65 del NF-κB reguló diversas citocinas relacionadas a la respuesta inflamatoria como la interleucina (IL)-1β, IL-6, IL-10, IL-17 y el factor de necrosis tumoral- α (TNF-α). Además de ejercer un efecto sobre el proceso fibrogénico, al regular la activación de las vías pro-fibrogénicas canónica y no canónica de las Smads, regula al factor de crecimiento transformante- β1 (TGF-β1), principal citocina profibrogénica. Ésta se encarga también de regular a la baja la proliferación, diferenciación, migración y apoptosis celular, y evita la activación de las células estelares hepáticas (HSC), encargadas del inicio de la fibrogénesis al perder su función de almacenar la vitamina A y adquirir la apariencia de miofibroblastos con capacidad proliferativa y fibrogénica después de incurrir en una lesión hepática. Resultados similares se encontraron en un modelo in vitro de co-cultivos de células recombinantes HepG2 (hepatocitos modificados) y HSC, las cuales fueron lesionadas con etanol y lipopolisacárido de bacterias. Estos co-cultivos expuestos a los tóxicos mencionados, incrementaron los genes relacionados con la fibrogénesis, tales como el α-SMA, TGF-β, PDGF y Smad3 y otros relacionados al proceso inflamatorio como el TNF-α, IL-6 y NF-κB. Sin embargo, al ser incubados con el esteviósido, estos genes fueron regulados a la baja. Por último, mediante un estudio in silico a través del acoplamiento molecular, se predijo que el esteviósido podría interactuar con los receptores TLR4-MD-2 y TNFR1, ambos ligados con el inicio de la inflamación al activar al NF-κB, evitando que los ligandos correspondientes puedan activar a estos receptores. En conclusión, el esteviósido presenta propiedades farmacológicas hepatoprotectoras a diversos niveles dentro de la lesión hepática. Además, al ser una molécula con un perfil de seguridad notable, se propone como candidato para ser estudiado en investigaciones clínicas en un futuro.
Sael Casas Grajales, oriundo de Acatlán de Pérez Figueroa, Oaxaca, es Licenciado en Químico Farmacéutico Biólogo por la Universidad Veracruzana en el 2012. Realizó sus estudios de Maestría y Doctorado en el Departamento de Farmacología, Cinvestav-Unidad Zacatenco, bajo la tutela del Dr. Pablo Muriel de la Torre (Investigador Cinvestav 3E, SNI III) en el laboratorio de Hepatología Experimental. Durante sus estudios de posgrado investigó moléculas de origen natural con potencial farmacológico como posibles agentes hepatoprotectores principalmente en modelos murinos.