La proteína ZO-2 contiene muchas regiones de unión con otras proteínas, por lo que se denomina proteína adaptadora o plataforma. Esto significa que tiene la capacidad para reunir una gran cantidad de proteínas en los sitios donde se encuentra. ZO-2 en las células epiteliales se halla en la porción citosólica de los contactos célula-célula llamados Uniones Estrechas (UEs). Allí funciona como plataforma que conecta a las proteínas integrales de la UE con el citoesqueleto de actomiosina. ZO-2 también se localiza en el núcleo y tiene en su secuencia señales para entrar y salir de este compartimento.
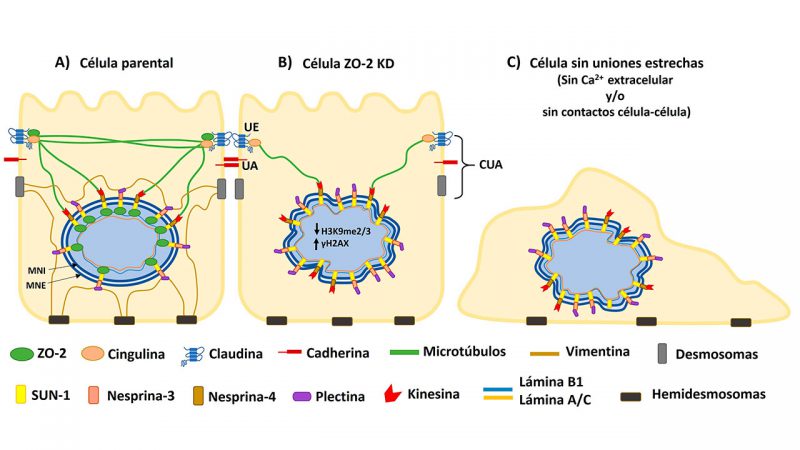
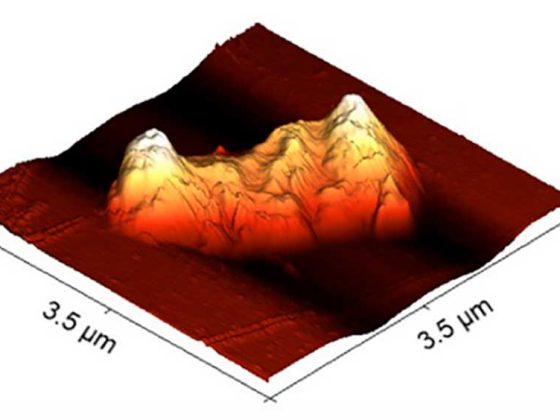
Como estrategia experimental para entender la función de ZO-2, se eliminó la expresión de esta proteína en las células epiteliales MDCK empleando un conjunto de ARNs interferentes que inhiben la traducción específica del ARN mensajero de ZO-2 (MDCK ZO-2 KD). El resultado fue que se alteró la forma del núcleo. Por microscopía electrónica, el núcleo de las células MDCK ZO-2 KD en lugar de verse con una morfología ovoide, aparece con lobulaciones, y por inmunofluorescencia el borde nuclear detectado con anticuerpos contra la proteína lamina B1 del nucleoesqueleto, presenta múltiples indentaciones.
La forma del núcleo es resultado del equilibrio entre la organización de la cromatina y el estado del nucleoesqueleto. La cromatina se refiere a la manera en la que el ADN se organiza en el núcleo al asociarse con las histonas. Cuando estas proteínas se modifican por metilación o acetilación, se altera la manera como el ADN se empaca. Así por ejemplo, las histonas metiladas se unen con mayor afinidad al ADN, lo que aumenta su compactación y bloquea la transcripción de genes. La eucromatina es la forma relajada de la cromatina que permite la transcripción de genes y que se distribuye de forma difusa en el núcleo. La heterocromatina en cambio, es la forma condensada de la cromatina que reprime la transcripción de genes y se localiza en la periferia nuclear donde ayuda a mantener la forma del núcleo. Cuando en las células MDCK ZO-2 KD se analizó la cromatina, se vio que en comparación con las células que si expresan a ZO-2, disminuyó la metilación de la histona 3. Esto indica que en las células carentes de ZO-2 bajó el contenido de heterocromatina, lo que sugiere que sus núcleos son más frágiles.
Por otro lado, al analizar al nucleoesqueleto de láminas A/C y B1 no se encontró alteración en las células ZO-2 KD. Se sabe que el nucleoesqueleto de láminas se asocia con el citoesqueleto de actina, microtúbulos y filamentos intermedios a través de proteínas del complejo LINC como SUN, que atraviesa a la membrana nuclear interna (MNI), y mediante su porción nucleoplásmica se une con las láminas. Asimismo, en el espacio entre la MNI y la externa (MNE), SUN se une a otras proteínas del complejo LINC llamadas nesprinas que cruzan la MNE. En el citoplasma, la nesprina-3 a través de la plectina se vincula con los filamentos de vimentina y la nesprina-4 se une a los microtúbulos por medio de kinesina.
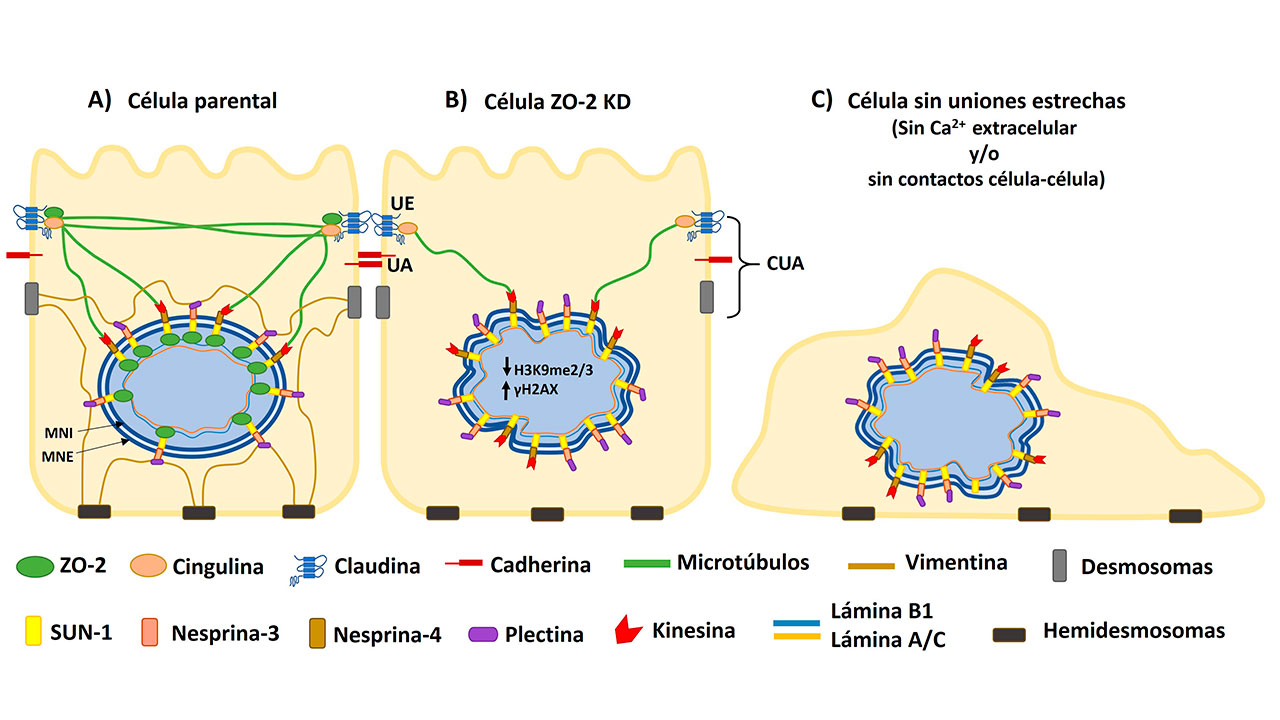
En las células MDCK parentales se vio que ZO-2 se conecta tanto a la lámina B1 como a la proteína SUN-1, lo que indica que ZO-2 funciona como un puente entre el nucleoesqueleto y el complejo LINC. Cuando las células carecen de ZO-2 no se establece una conexión adecuada entre el nucleoesqueleto y el citoesqueleto y esto se manifiesta por la aparición de una red inestable de microtúbulos. Igualmente, la falta de ZO-2 provoca la desaparición de la red de vimentina que rodea al núcleo y da resistencia mecánica a este organelo. Estos cambios tienen un efecto deletéreo en el núcleo pues además de alterar su forma dañan su resistencia a la presión mecánica. Por ello, en las células MDCK ZO-2 KD aumentan las rupturas en la doble cadena del ADN, evaluadas por un aumento en la expresión de focos nucleares de fosforilación de la histona H2AX, responsable de activar la respuesta al daño al ADN.
Ya que ZO-2 está presente tanto en el núcleo como en las UEs, nos preguntamos si era necesaria la presencia de estas uniones para mantener la forma del núcleo. Para ello, se sembraron células parentales en dos condiciones en las que no se pueden formar UEs: un medio con bajo calcio (1-5 μM) o muy baja densidad. Se observó que si las células no pueden formar uniones célula-célula por falta de calcio en el medio o por ausencia de células vecinas con las que contactarse, el núcleo se lobula y exhibe múltiples indentaciones, de manera similar a lo observado en los núcleos de las células ZO-2 KD. Por ello, se concluye que en las células epiteliales se requiere de ZO-2, calcio extracelular y contactos célula-célula para mantener la forma nuclear (Hernández-Guzmán et al., 2021).
En conjunto, estas observaciones indican que la forma del núcleo en los epitelios depende de establecer UEs y mantener una óptima conexión entre el nucleoesqueleto de láminas y el citoesqueleto de vimentina y microtúbulos que rodea al núcleo, a través de ZO-2 y el complejo LINC.
Referencia
- Hernández-Guzmán, C., Gallego-Gutiérrez, H., Chávez-Munguía, B., Martín-Tapia, D., and González-Mariscal, L. (2021) “Zonula occludens 2 and cell-cell contacts are required for normal nuclear shape in epithelia”. Cells 10:2658