La diabetes mellitus es un grupo de enfermedades metabólicas caracterizadas por hiperglucemia, las cuales son el resultado de defectos en la secreción o la acción de la insulina (PROY-NOM-015-SSA2-2018). Dentro de estas patologías, la diabetes mellitus tipo 2 (DM2) es una enfermedad que se caracteriza por la pérdida progresiva de la secreción de insulina por las células b pancreáticas y se acompaña de resistencia a la insulina (PROY-NOM-015-SSA2-2018). La función principal de la insulina es contrarrestar la acción concertada de varias hormonas que inducen hiperglicemia y mantener normales los niveles de glucosa en la sangre. Además de su papel en la regulación del metabolismo de la glucosa, la insulina estimula la lipogénesis, disminuye la lipólisis, y aumenta el transporte de aminoácidos en las células (Bergam et al., 2002).
La resistencia a la insulina (RI) es una condición en la cual, la insulina produce una respuesta menor a la esperada sobre sus tejidos blancos (hígado, músculo en reposo, tejido adiposo); por consiguiente, condiciona un incremento en las concentraciones de la insulina sérica (hiperinsulinemia) para compensar la falta de acción de esta hormona. La RI se ha asociado con un aumento significativo de la morbimortalidad cardiovascular y un factor de riesgo para DM2.
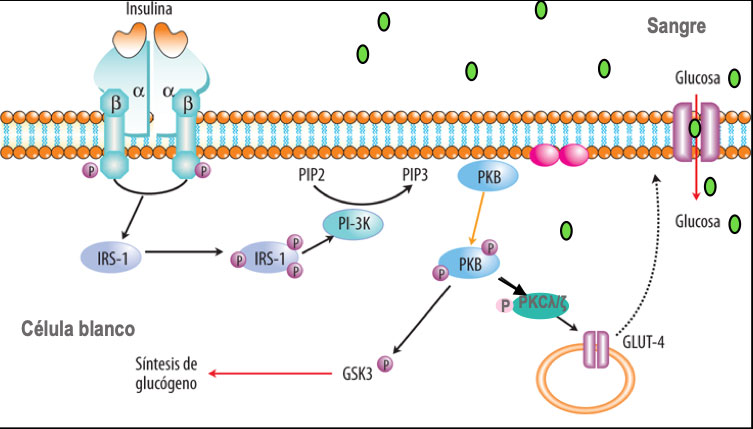
La insulina, al unirse a su receptor sobre la superficie de las células blanco, induce a que las vesículas que contienen los transportadores GLUT-4 se transloquen a la superficie de la célula y entonces se transporte la glucosa en la sangre hacia el interior de la célula (fig1). Por lo que la resistencia a la insulina se debe a alteraciones en varios puntos de la cascada de señalización del receptor de la insulina presente sobre la superficie de la célula por diversos mecanismos, lo que conlleva a que los transportadores GLUT-4 no sean translocados a la membrana celular; ello resulta en un aumento en las concentraciones séricas de glucosa fig. 1. El páncreas responde a estas altas concentraciones de glucosa sérica produciendo más insulina, lo que conlleva a una disminución de la funcionalidad de la célula b pancreática, la cual en algún momento deja de producirla.
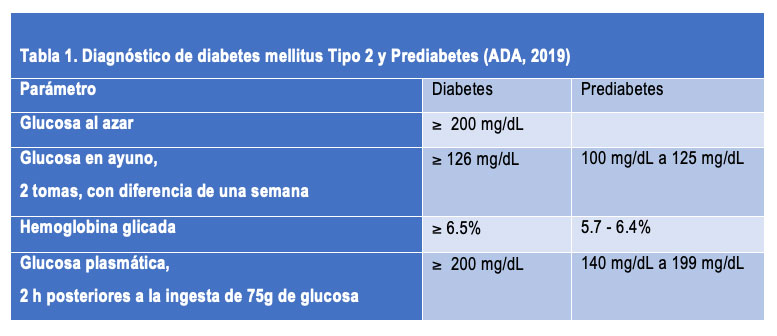
A pesar de la gran importancia de la insulina en la regulación de la toma de la glucosa por las células para mantener las concentraciones adecuadas en la sangre, el diagnóstico de la diabetes continúa siendo glucocéntrico (Tabla1).
Varios estudios han mostrado que el determinar en un sujeto la concentración de la insulina en la sangre, además de la glucosa, permite identificar la sensibilidad a la insulina y estimar la función de las células β a través de un índice denominado HOMA 2 (The Homeostasis Model Assessment 2). Con estas dos concentraciones es posible establecer el HOMA IR (de resistencia a la insulina) y HOMA B (función de la célula β), los cuales se determinan utilizando un programa de acceso libre de la Universidad de Oxford, Inglaterra, en el que se introducen los datos de glucosa e insulina https://www.dtu.ox.ac.uk/homacalculator/ . Se considera a un sujeto con RI cuando tiene un HOMA IR ³ 2.6; a un sujeto sano con un HOMA B del 100% y con Diabetes Mellitus con un HOMA B £ 60% (Levy et al., 1998)
La diabetes tipo 2 es uno de los padecimientos más prevalentes en México. La más reciente estadística de ENSANUT (2016) mostró que la prevalencia era del 9.4% en la población adulta (10.3% en mujeres y 8.4% en los hombres). Además, se observó un incremento en la prevalencia de la DM2 de manera constante del 2000 al 2012, particularmente en dos grupos etarios, el de 20 a 29 años y el de 50-59 años, pasando del 0.4 al 1.6% y del 10.0 al 19.4%, respectivamente. Es una enfermedad que está asociada con varias complicaciones las cuales tienen un gran impacto en la salud. La DM2 es una de las principales causas de ceguera, insuficiencia renal crónica y amputaciones no traumáticas, y es una de las 10 causas más frecuentes de hospitalización en adultos (Rojas-Martínez et al 2018). También los pacientes con DM2, tienen un mayor riesgo de sufrir infarto del miocardio o cerebral y explica el 30% de la mortalidad (Rojas-Martinez et al., 2018). Por otra parte, se ha estimado que el tratamiento de la DM2 genera para los sistemas de salud un gasto de aproximadamente 85 mil millones de pesos al año. (https://www.animalpolitico.com/sin-competitividad-no-hay-paraiso/kilos-de-mas-pesos-de-menos-el-costo-de-la-obesidad-en-mexico/#_ftn2).
Por todo lo anterior es claro lo indispensable que es entender la fisiopatología de la DM2, para identificar a los sujetos en riesgo de desarrollar la enfermedad mucho antes de que la presenten y así cambiar la política de salud hacia la prevención e identificación de sujetos en riesgo de desarrollar este padecimiento. Hasta el momento se han identificados varios factores de riesgo, siendo el de presentar prediabetes (Tabla 1) el de mayor posibilidad de desarrollar la enfermedad, ya que se ha observado que del 5% al 10% de los sujetos con prediabetes desarrollan DM2 al año de diagnóstico así como el 70% de las personas con prediabetes desarrollaran DM2 en algún momento de su vida (Villanueva-Sosa et al., 2015). Como se muestra en la Tabla1, se define a los prediabéticos nuevamente sólo con base en un diagnóstico glucocéntrico (Tabla 1).
Con el fin de identificar las características de individuos con riesgo de desarrollar DM2 realizamos un estudio piloto donde se reclutaron sujetos de 18 a 75 años (sanos) que no fueran hipertensos, diabéticos ni tuvieran insuficiencia cardiaca, renal, hepática, enfermedades reumatológicas/inmunológicas o enfermedades infecciosas. Se reclutaron un total de 273 sujetos a los cuales se les determinó la glucosa, insulina y el perfil de lípidos en ayuno; se tomaron sus datos antropométricos, presión arterial, se realizó una historia clínica y se les determinó el HOMA 2. En la Tabla 2 se muestra los sujetos con y sin resistencia a la insulina (RI).
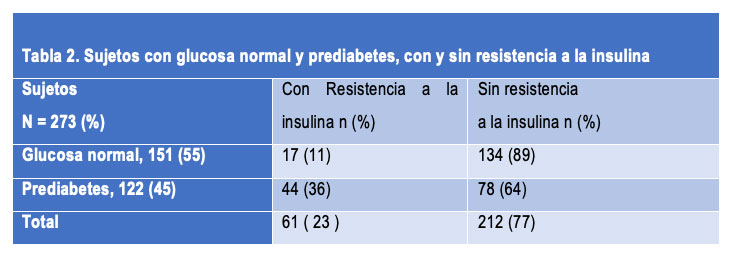
Es claro que es necesario realizar estudios de cohorte que nos permitan determinar cuál es la progresión de los sujetos con RI y establecer si debemos considerarlos sujetos con un mayor riesgo de desarrollar diabetes, ya que identificamos que el 11% de los sujetos sin glucosa alterada en ayuno presentan RI además de un mayor riesgo de eventos cardiovasculares. Con base en encuesta Intercensal 2015 se estimó que para el 2018 tendríamos una población ³ de 18 años de aproximadamente 86 millones 700 mil, por lo que potencialmente tendríamos que cerca de 9.5 millones (11%) de personas podrían tener RI y por ende, potencialmente estar en riesgo de desarrollar DM2 y eventos cardiovasculares. Estos resultados muestran la importancia de determinar la insulina y el HOMA2 como pruebas de rutina para identificar la población en riesgo de desarrollar estas enfermedades.
Referencias
- American Diabetes Association (ADA). Standards of Medical Care in Diabetes. 2. Classifications and Diagnosis of Diabetes (2019). Diabetes Care, 42 (S1), S13-S28.
- Bergman, R. N., Finegood, D. T., & Kahn, S. E. (2002). The evolution of β‐cell dysfunction and insulin resistance in type 2 diabetes. European journal of clinical investigation, 32, 35-45.
- Levy JC, Matthews DR, Hermans MP (1998). Correct homeostasis model assessment (HOMA) evaluation uses the computer program (Letter). Diabetes Care, 21, 2191-2192.
- Rojas-Martínez, R., Basto-Abreu A., Aguilar-Salinas C.A., Zarate-Rojas E., Villalpando S., & Barrientos-Gutiérrez T. (2018). Prevalencia de diabetes por diagnóstico médico previo en México. Salud Pública de México, 60(3), 224-232
- Villanueva-Sosa, L. G., Cordero-Franco, H. F., & Salinas-Martínez, A. M. (2015). Prevalence of Prediabetes Based on Fasting Plasma Glucose and Glycosylated Hemoglobin in an At-Risk Mexican Population. Metabolic Syndrome and Related Disorders, 13(8), 352–355
Diana Helena Ramírez-Velasco1,2, César Iván Elizalde-Barrera1,2, Catalina López-Saucedo1, Alberto F Rubio-Guerra4, Teresa Estrada-García1*
Departamento de Biomedicina Molecular, Centro de Investigación y de Estudios Avanzados, Instituto Politécnico Nacional (CINVESTAV-IPN), CDMX, México
2Hospital General Regional 1 Dr. Carlos Mac Gregor Sánchez Navarro, Instituto Mexicano del Seguro Social (IMSS), CDMX, México
3Hospital General de zona número 30, Instituto Mexicano del Seguro Social (IMSS), CDMX, México
4Jefatura de Enseñanza e Investigación, Hospital General de Ticomán, CDMX, México