Introducción
El agua es un recurso indispensable para todos los seres vivos por lo que tiene carácter de bien público. Es un insumo y, por otra parte, un bien básico en la generación de riqueza, debido a que es utilizada en muchos procesos productivos. Los problemas asociados con este líquido son severos en todo el mundo. En muchas regiones la disponibilidad natural del agua es crítica, su calidad es inapropiada y el tratamiento del agua residual es insuficiente1. La mala calidad del agua se relaciona con su contaminación, que puede ser natural, o producto de la descarga de aguas residuales sin tratamiento, sean de origen doméstico, industrial, agrícola, pecuario o minero. La contaminación del agua puede presentarse en cualquier espacio que la alberga: ríos, lagos, acuíferos e incluso el mar2.

En años recientes ha surgido preocupación por la presencia de contaminantes denominados “emergentes” (Figura 1), entre los que se incluyen productos farmacéuticos, de cuidado personal, agentes tensoactivos, plastificantes, aditivos industriales y microplásticos, la mayor parte constituidos por moléculas orgánicas. Además de estos también se incluyen nanopartículas de plata, oro y, óxidos metálicos, entre otros, en los cuales se tienen que utilizar otro tipo de tratamientos para su eliminación 3.
Descripción de la molécula de agua
La molécula de agua, H2O, es una de las moléculas más simples y estables, formada por un átomo de oxígeno, unido covalentemente a dos átomos de hidrógeno, lo que significa que los electrones en el enlace entre el oxígeno y los hidrógenos se comparten entre ellos. El oxígeno es un átomo muy electronegativo lo cual significa que tiende a atraer a los electrones de los átomos en un enlace (en este caso, a los del hidrógeno), por su parte el hidrógeno es muy poco electronegativo, por lo tanto, va a ceder con facilidad sus electrones. Esto hace que la densidad electrónica de la molécula de agua esté acumulada sobre el átomo de oxígeno dejando a los hidrógenos con carga parcial positiva como se observa en la Figura 2, o, dicho de otra forma, haciendo que el agua sea una molécula polar.
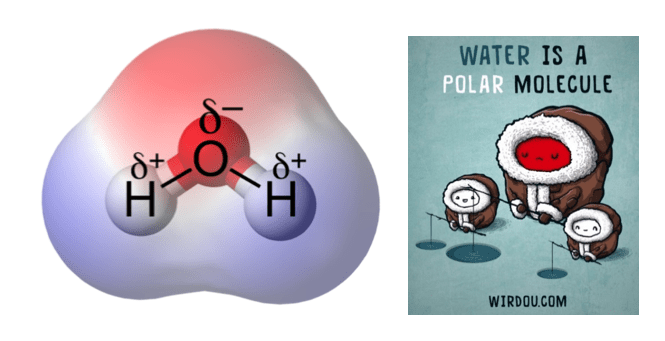
Figura 2. El agua es polar
El átomo de oxígeno tiene 6 electrones en su capa de valencia, es decir, 6 electrones con los que puede formar enlaces. Sin embargo, con los hidrógenos solo comparte dos de estos electrones, quedándose con cuatro sin compartir, agrupados en dos pares libres. Como estos pares no-compartidos se repelen y tienden a alejarse lo más posible entre sí, la molécula del agua tiene un peculiar ángulo de 104.5° en el enlace H-O-H, como se observó en la Figura 2. Cada átomo de oxígeno forma dos puentes de hidrógeno con las moléculas vecinas y de este modo, el agua forma una extensa red tridimensional donde cada átomo de oxígeno forma casi un tetraedro con cuatro átomos de hidrógeno, dos unidos por enlaces covalentes y dos por puentes de hidrógeno, como se esquematiza en la Figura 3.
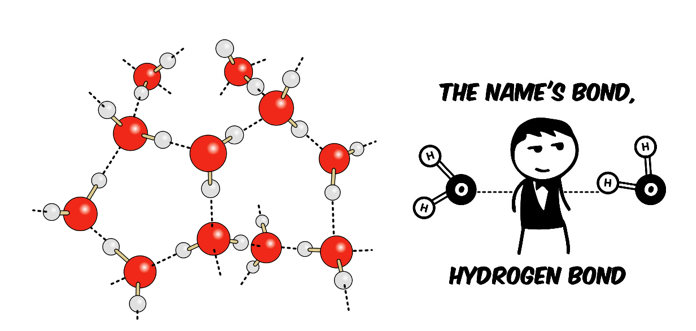
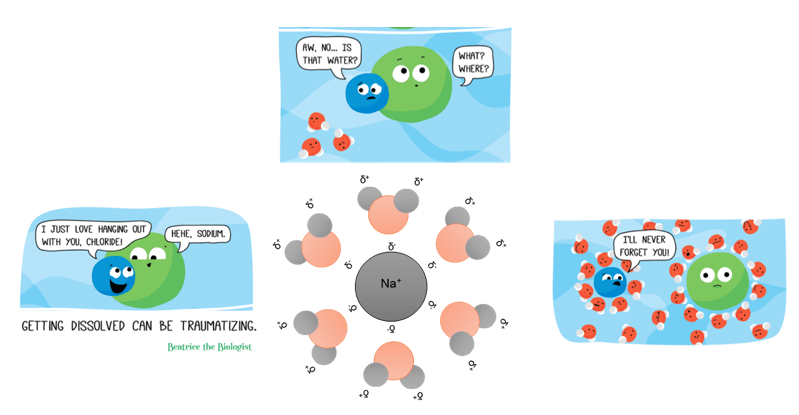
Ninguna otra molécula tiene capacidad para formar estas redes de puentes de hidrógeno, y es la causa de la estabilidad del agua líquida, su alto punto de ebullición con respecto a moléculas de tamaño similar, su polaridad y su cualidad como solvente de una gran cantidad de compuestos. La solubilidad se relaciona con las atracciones entre las moléculas del disolvente (en este caso del agua) con las moléculas o iones del soluto (la sustancia que se disuelve en el agua). El dicho “lo semejante disuelve a lo semejante” es de gran ayuda para predecir la solubilidad de una sustancia en determinado disolvente 4, por lo que es de esperarse que el agua tenga una mayor afinidad por sustancias polares, o sustancias iónicas. Por ejemplo, el cloruro de sodio o sal de mesa tiene una alta solubilidad en agua ya que es un compuesto iónico. Como se muestra en la Figura 4, el agua rodea a los iones sodio con carga positiva (cationes) orientando su extremo negativo hacía dicho ion; lo mismo ocurre con el ion cloruro que tiene carga negativa (anión), solo que en este caso es el polo positivo del agua el que se orienta hacía el anión. Este proceso se conoce como solvatación.
Contaminación del agua
La alta solubilidad de sustancias polares y la solvatación debido a su carácter dipolar; su geometría y la formación de puentes de hidrógeno debido a la distribución de sus electrones enlazantes y no enlazantes y su comportamiento anfótero, es decir, como ácido o como base, explican por qué el agua se contamina tan fácilmente y también sirve de punto de referencia para generar estrategias de remoción de contaminantes de este líquido.
Aguas residuales
En el ámbito mundial entre 85 y 95% del agua residual se descarga directamente a los ríos, lagos y océanos sin recibir tratamiento previo5. Se estima que entre 2014 y 2015 cada mexicano generó alrededor de 60 metros cúbicos de aguas residuales al año, ¡algo así como la capacidad de un contenedor marítimo!

Tratamientos de aguas residuales
Las aguas residuales presentan diferente composición, dependiendo de su origen. Las de origen urbano están constituidas principalmente por desechos humanos y animales (contaminación fecal), y domésticos (grasas, detergentes), entre otros; mientras que las aguas residuales de origen industrial presentan diversas composiciones, de acuerdo con el proceso productivo de procedencia.
El tratamiento de aguas se lleva a cabo mediante operaciones ya sea físicas, químicas, o biológicas. El objetivo de este proceso es eliminar los contaminantes de origen natural, industrial, doméstico, entre otros que están presentes en el agua. Es importante tomar en cuenta también el tipo de contaminantes que contiene un agua residual para tomar una decisión acerca del tratamiento más conveniente2.
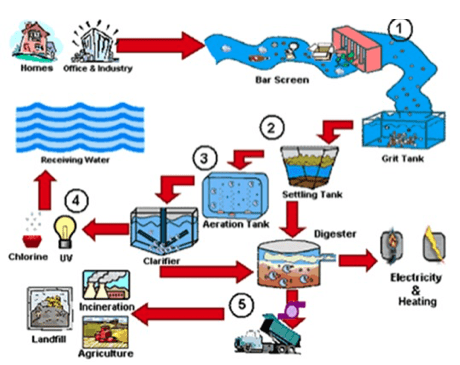
Los sistemas de tratamiento de aguas residuales en general se dividen en 3 etapas:
1) Tratamiento primario. Son procesos físicos o químicos que tienen como objetivo eliminar el contenido de sólidos. Los procesos físicos son aplicados al agua con contaminantes inorgánicos o con materia orgánica no biodegradable o insoluble (en suspensión); por su parte, los procesos químicos son usados para la eliminación de sustancias solubles, empleando agentes químicos como floculantes o coagulantes, que mejoran la separación de partículas 6.
2) Tratamiento secundario. Su función es la degradación de materia orgánica presente en el agua residual, empleando microorganismos que la utilizan como nutriente.
3) Tratamiento terciario. Tiene como objetivo eliminar compuestos específicos que no pudieron ser eliminados en los sistemas anteriores. La cloración y ozonización para eliminar organismos patógenos, así como la adsorción (con carbón activado) para eliminar compuestos organoclorados son ejemplos de algunos procesos que pueden ser aplicados en esta etapa.
Sistemas alternativos de tratamiento de aguas residuales
Existen diversos métodos y técnicas para la remoción de compuestos orgánicos de difícil tratamiento, como residuos farmacéuticos y cosméticos, metales pesados, colorantes, compuestos organoclorados y pesticidas. Esto ha propiciado el desarrollo de nuevas técnicas para el tratamiento de agua, entre las cuales destacan i) la filtración por membranas, que consiste en separar dos flujos, agua permeada o filtrada y un rechazo que contiene las partículas y sales concentradas que se han eliminado del flujo de agua de alimentación al equipo; ii) los sistemas naturales de tratamiento que utilizan conceptos hidráulicos, microbiológicos o biológicos para simular y controlar los procesos físicos, químicos y biológicos que ocurren en los humedales naturales; y iii) los procesos avanzados de oxidación o PAO (por sus siglas en inglés), que se pueden definir como técnicas de tratamiento basadas en la acción de especies altamente reactivas, los radicales hidroxilos, que conducen a la oxidación completa de los contaminantes. Entre estos últimos se encuentra la fotodegradación que se define como la transformación química de los contaminantes en sustancias inocuas, acelerada por efecto de la radiación UV, visible o infrarroja en la presencia de una sustancia, llamada fotocatalizador, que absorbe los fotones y genera las especies altamente reactivas 7,8.
Fotocatálisis
Como se mencionó, la fotocatálisis es un proceso avanzado de oxidación en el que la luz facilita reacciones químicas en la superficie de un material llamado fotocatalizador que puede servir para destruir contaminantes presentes en el medio, pero también sirve para generar hidrógeno e incluso electricidad 7. Inicia con la generación de portadores de carga, lo que ocurre cuando el fotocatalizador, que usualmente es un material semiconductor de tamaño nanométrico, como el TiO2, es iluminado con la radiación de la energía apropiada. La energía que recibe el fotocatalizador se convierte en un par de partículas cargadas, una positiva, el hueco (h), y la otra negativa, el electrón, como se muestra en la siguiente ecuación:
TiO2 + hν ↔ h+ + e– Ec. (1.1)
Al alcanzar la superficie del material, el hueco y el electrón reaccionan con el oxígeno molecular (O2) para formar el radical superóxido (O2.-) y con el agua, para formar el radical hidroxilo (OH.). Estas especies altamente reactivas son las que oxidan a los contaminantes presentes en el agua, como se esquematiza en la Figura 7 9.
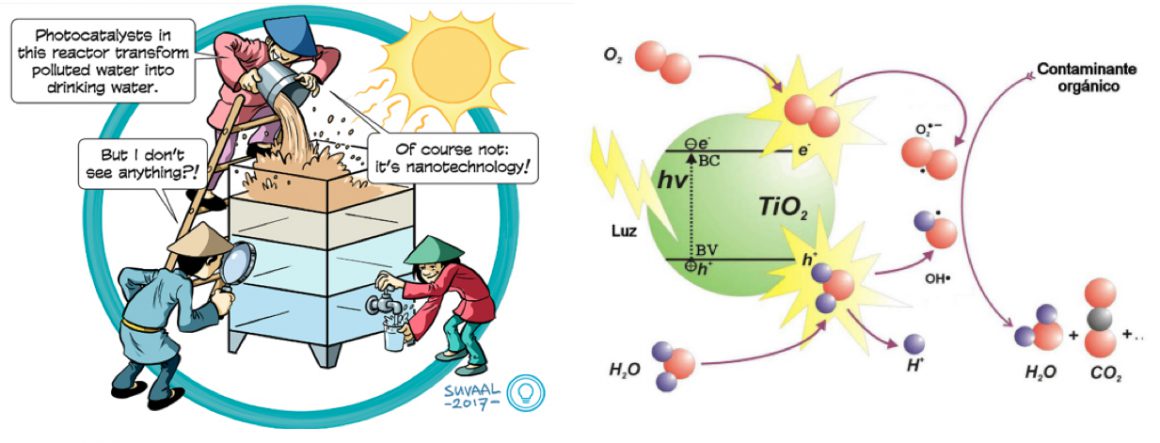
Fotocatalizadores soportados
Los fotocatalizadores como el TiO2 se suelen utilizar suspendiendo los polvos en las aguas contaminadas, por lo que, para recuperarlos después de tratar el agua, se requiere un paso de filtración, lo que consume tiempo y energía. El polvo es difícilmente recuperable y en vez de ayudar a la descontaminación del agua se vuelve parte de los contaminantes emergentes. Debido al pequeño tamaño de las partículas de TiO2, que es de menos de 0.5 µm para los aglomerados y generalmente de 10 a 100 nm para las partículas elementales, la separación completa es muy difícil y costosa, por lo que el proceso no es viable a gran escala. Para dar solución a este problema, se ha propuesto soportar el TiO2 en diferentes materiales como el vidrio, cuarzo, espumas cerámicas y piedras porosas, entre otros.
Fotocatalizadores soportados por impresión 3D
La impresión 3D es una tecnología que en años recientes ha revolucionado la manufactura, pero también ha encontrado aplicación en campos de la salud y del medio ambiente. La impresión 3D consiste en utilizar filamentos o polvos de polímeros o de metales, y fundirlos con un resistor, con láser o con plasma en una boquilla que se mueve en el plano X-Y y que se desplaza en el eje Z conforme se añade capa por capa del material fundido, que se solidifica para formar la pieza 3D que se diseña en la computadora. ¡Con esta tecnología se está pensando en imprimir hasta órganos artificiales!

La obtención de materiales para impresión 3D con comportamiento fotocatalítico se ha realizado de distintas maneras, por ejemplo: utilizando soluciones precursoras de sol-gel basadas en un alcóxido de titanio y material polimérico como aditivo; también con deposición robotizada de precursores organometálicos del mismo óxido sobre estructuras de polímero y por medio de mezclas de polvos TiO2-polímero mediante fundición que son utilizadas como filamentos para las impresoras10.
Fotocatalizadores soportados en el Instituto Politécnico Nacional
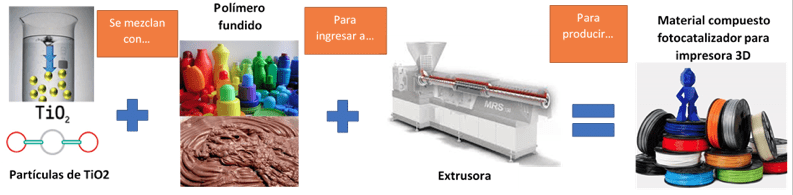
En el proyecto que estamos desarrollando en las unidades Querétaro y Altamira del CICATA IPN, se propone obtener materiales compuestos, polímero-TiO2, como se esquematiza en la Figura 9. Se sintetizarán partículas de TiO2 con el método sol-gel variando los tiempos de envejecimiento para obtener nanopartículas de diferente tamaño y se mezclarán diferentes proporciones de partículas de TiO2 con distintos polímeros fundidos para obtener filamentos por extrusión. Con ellos se fabricarán por impresión 3D diversas formas que se adapten a un reactor, para su aplicación en la degradación de contaminantes orgánicos persistentes.
Perspectiva
- Los procesos de oxidación avanzada como la fotocatálisis prometen contribuir a dar una solución eficiente y novedosa para solucionar problemas de contaminación en cuerpos de agua.
- La impresión 3D permitirá crear piezas a la medida, en las que el TiO2 limpiará el agua contaminada mientras el polímero lo detiene.
Para indagar más…
- Carabias, J. & Lavanda, R. Agua, medio ambiente y sociedad. Universidad Nacional Autónoma de México : El Colegio de México : Fundación Gon- zalo Río Arronte, 2005. (2005). doi:10.1088/1751-8113/44/8/085201.
- Agua.org.mx. Contaminación en México. https://agua.org.mx/agua-contaminacion-en-mexico/ (2018).
- Fundación Aquae. Microplásticos en la tierra, en el agua dulce y en el mar. https://www.fundacionaquae.org/dia-mundial-del-medio-ambiente-microplasticos-en-la-tierra-en-el-agua-dulce-y-en-el-mar/ (2020).
- Goldsby, K. A. & Chang, R. Química, Williams College, Florida State University. (2009).
- SEMARNAT. Capitulo 6 Agua. Inf. la situación del medio Ambient. en México 363–429 (2015).
- Comisión Nacional del Agua (CONAGUA). Manual de agua potable, alcantarillado y saneamiento: Sistemas alternativos de tratamiento de aguas residuales y lodos producidos. (2007).
- CINVESTAV. FOTOCATÁLISIS Y GRAFENO : ¿ ADIÓS A LA CONTAMINACIÓN ? Av. Y Perspect. 6, (2020).
- TECSPAR. Manual de tecnologías sostenbles en tratamiento de aguas. (2006).
- Luis Alejandro, A. S. Síntesis de dióxido de titanio nanoestructurado para la degradación de azul de metileno Tesis. (CICESE, 2018).
- Elkoro, A., Soler, L., Llorca, J. & Casanova, I. 3D printed microstructured Au/TiO2 catalyst for hydrogen photoproduction. Appl. Mater. Today 16, 265–272 (2019).













2 comentarios
Exelente Piblicacion , Gran Avance en el medio Cientifico…. Muchas Felicidadez atodos los que Participaron …. 🙂
Hola Rosi, muchas gracias a ti por tu gran apoyo.
Te mando un abrazo
Comentarios no permitidos.